췌관내 유두상 점액종양으로 오인된 췌장의 신경내분비종양 1예
요약
췌장의 신경내분비종양은 매우 드문 종양이나 최근 영상검사가 발전하면서 진단 빈도도 증가하고 있다. 하지만 세로토닌 분비 신경내분비 종양은 매우 서서히 진행하고 임상 양상이 뚜렷하지 않아 진단에 어려움이 있다. 영상검사에서 폐쇄 병변 없이 췌관 확장만 7년 동안 서서히 진행하여 췌관내 유두상 점액종양으로 의심하였던 환자에서 세로토닌 분비 신경내분비종양으로 수술 후 뒤 늦게 진단하였기에 이를 보고하는 바이다.
Keywords: 신경내분비종양, 세로토닌, 췌관확장
Abstract
Neuroendocrine tumors of the pancreas are exremely rare tumors, but recent imaging examination advances, diagnostic frequency is also increasing. However, there is difficulty of diagnosis of pancreatic serotonin producing neuroendocrine tumors, because tumors grow slowly and clinical symptoms are not significant. A 60-year-old male patient with pancreatic duct dilatation progresses gradually during the seven years without obstructing lesion in imaging studies, we suspected the mass as intraductal papillary mucinous neoplasm. However, we diagnosed his case as neuroendocrine tumor after surgery and report here with literature review.
Keywords: Neuroendocrine tumor, Serotonin, Pancreatic duct dilatation
서 론
신경내분비종양(Neuroendocrine tumors)은 정상적으로 분포하는 다양한 신경내분비세포(enterochromaffin cells or Kulchitsky cells)로부터 기원하여 신경내분비 분화를 하는 상피 종양으로[ 1] 여러 장기에서 발생할 수 있으나 위장관, 췌장, 폐에 주로 발생한다[ 2]. 생물학적 성상에 따라 유암종(carcinoid tumor), 도세포종(islet cell tumor), 신경아세포종(neuroblastoma), 폐 및 폐외 소세포암(small cell carcinoma)등으로 구분되며 매우 다양한 임상적 특징을 가진다[ 3]. 췌장의 신경내분비종양은 췌장에서 발생하는 종양의 1-2%를 차지하며 발생빈도는 인구 10만 명당 1명 이하인 드문 종양이다[ 4]. 인슐린종, 가스트린종, 글루카곤종, 소마토스타틴종과 같이 호르몬의 과다분비를 일으켜 증상이 나타나는 기능성 종양과 임상증상이 없는 비기능성 종양으로 나뉘어지는데, 비기능성 종양은 커진 종괴 또는 원격 전이로 진행된 상태에서 진단되기도 하지만[ 5], 영상검사를 통해 우연히 발견되기도 한다[ 6]. 저자들은 유두상 점액종양으로 진단하여 수술하였으나 췌관 폐쇄 원인이 발견되지 않을 정도의 매우 작은 세로토닌분비 신경내분비 종양으로 최종 진단한 예가 있어 문헌고찰과 함께 보고하는 바이다.
증 례
60세 남자 환자가 6개월 전부터 지속된 좌상복부 통증을 주소로 타 병원에서 복부 초음파 검사 후 5 cm 크기의 췌장낭성 종괴가 발견되어 본원으로 전원되었다. 과거력에서 당뇨병, 뇌경색, 만성 신부전, 울혈성 심부전, 심방 세동을 진단받고 치료 중이었고 20년 전 담낭절제술을 받았고, 7년 전 좌측 부신 선종으로 좌측 부신 절제술을 받았다. 사회력상 흡연력은 없었으나 주 1회 소주 0.5병의 음주력이 있었다.
방문 당시 의식은 명료하였으며, 이학적 검사에서 입원 당시 활력징후는 혈압 120/80 mmHg, 맥박 72회/분, 호흡수 18회/분, 체온 36.7℃였다. 공막 황달은 관찰되지 않았으며 복부진찰에서 장음은 정상이었고, 좌상복부에 경한 압통이 있었으나 반발 압통은 없었다. 복부에서 촉지되는 종괴는 없었다. 검사실 소견에서 백혈구 4,400/mm3, 혈색소 13.2 g/dL, 혈소판 201,000/mm3였고, 혈청 생화학 검사에서 총 단백 8.0g/dL, 알부민 4.2 g/dL, 아스파라진산 아미노전이효소(AST) 16 IU/L, 알라닌 아미노전달효소(ALT) 11 IU/L, 알칼리성 인산분해효소(alkaline phosphatase) 58 U/L, 총 빌리루빈 0.46 mg/dL, 아밀라아제 58 U/L, CA 19-9 26 U/mL로 정상이었다. 혈중 요소 질소 42.1 mg/dL, 크레아티닌 1.8 mg/dL로 증가되어 있었으나 최근 1년 동안 큰 차이는 없었다.
7년 전 좌측 부신 선종 진단 당시 시행했던 복부 전산화단층촬영에서 췌장 종괴 없이 췌장 체부부터 미부까지 경도의 미만성 주췌관 확장만 관찰되었으나 이후 추적검사는 하지 않았었다. 내원하여 시행한 자기공명담췌관조영술(magnetic resonance cholangiopancreatography)에서 주췌관은 체부에서 미부까지 심한 미만성 확장을 보이고 체부에서는 직경 3.4 cm 낭성 확장을 보였으나 췌장 두부(머리부분)의 췌관에서 이상소견은 관찰되지 않았다( Fig. 1). 내시경초음파검사에서도 췌장 두부와 체부 사이의 췌관 확장 이행부에 종괴는 관찰되지 않았으나 확장된 미부 췌관 내에서는 결절성 병변이 관찰되었다( Fig. 2A). 췌관의 심한 낭성 확장에 대해서 침윤성 췌관내 유두상 점액종양 의심 하에 췌장 전절제술을 시행하였다. 수술 소견에서 췌장 체부의 실질은 위축이 매우 심하고 늘어난 췌관은 종괴 모양으로 관찰되었다( Fig. 2B). 수술 검체 절단면에서 췌관 내에 종괴성 병변은 발견되지 않았으나, 현미경 검사에서는 0.8 × 0.7 × 0.5 cm 크기의 작은 결절성 병변이 췌장 두부에서 관찰되었다. 이 병변은 췌관을 압박하고 있었고 이로 인해 췌관 확장과 기질성 섬유화(stromal fibrosis)가 동반되어 있었으며 췌관 상피는 정상이었다( Fig. 3A- C). 종양세포들은 풍부한 세포질과 작고 둥근핵을 가지고 소(nest) 구조로 관찰되었다( Fig. 3D). 면역조직화학 염색에서 CD56, synaptophysin, chromogranin 양성이었으며, 추가로 시행한 세로토닌 염색에서도 양성으로( Fig. 4) 세로토닌 분비 신경내분비종양으로 진단되었다. Ki-67 지수는 1% 미만이었고 10군데의 고배율에서 유사분열은 관찰되지 않았다. 환자는 수술 후 합병증 없이 퇴원하였고 현재 외래에서 추적관찰 중이다.
고 찰
췌장의 신경내분비종양은 악성에 대한 잠재력을 가지고 있는 비교적 드문 종양으로 최근 빈도가 점차 증가하여 국내에서는 신경내분비종양 발생률이 30년 동안 4배 정도 증가하였고 미국과 유럽에서도 20배 정도 증가하는 추세를 보이고 있다[ 6, 7]. 일반적으로 췌장 신경내분비종양은 복부 전산화 단층촬영 및 자기공명 영상검사에서 조영증강이 잘되는 종괴로 관찰되며[ 8, 9] 췌관 폐쇄를 일으키는 경우는 매우 드물고 특별한 증상없이 여러 가지 목적으로 시행한 복부 영상 검사를 통해 우연히 발견되는 경우가 많다[ 10]. 본 증례에서 췌장 두부의 췌관은 정상으로 췌관 폐쇄를 일으킬 수 있는 췌장 상피내 종양(pancreatic intraepithelial neoplasm)이나 작은 선암 또한 감별이 필요하였지만, 이미 7년 전부터 동반된 종양 없이 췌관의 미만성 확장만 보였고 본 영상검사상에서도 뚜렷하게 관찰되는 종양 없이 같은 부위의 주췌관 확장만 심해졌으며 췌관 내 결절도 동반되어 침윤성 췌관내 유두상 점액종양에 의한 췌관 협착 및 점액에 의한 췌관 폐쇄를 먼저 고려하였고, 유두부를 통한 점액유출 관찰 가능성은 적다고 판단하여 내시경적 역행성 담췌관조영술은 시행하지 않았다.
본 증례는 수술 후 발견된 신경내분비종양에 대해 세로토닌 염색을 추가로 시행하여 세로토닌 분비 신경내분비 종양으로 진단하였는데 폐나 위장관에서 카르시노이드 증후군을 일으키는 세로토닌 분비 신경내분비종양은 췌장에서 매우 드물게 보고되어 있다[ 11]. 종양이 매우 커져 다른 장기로 전이된 후 진단된 보고가 있으나[ 12] 대개 증상 없이 우연히 발견되거나 복통이나 체중감소 같이 세로토닌 분비와 관련 없는 증상으로 호소하는 환자에서 우연히 영상 검사에서 발견되었다[ 13]. 신경내분비종양에서 췌관확장이 발생하는 기전은 종양에 의한 췌관의 직접침윤과 직접침윤하지 않는 경우에는 크기가 작아도 장기간에 걸친 주변조직의 섬유화가 주췌관의 협착 및 폐색을 일으키고 이로 인해 췌관 확장과 실질의 위축이 동반된다고 알려져 있다[ 14, 15]. 본 증례의 경우, 이전 보고들과 달리 영상 검사에서 종양이 발견되지 않았는데 그 이유로는 매우 작은 크기의 결절성 병변이 췌관 침범 없이 췌관을 압박하고 있어 폐쇄 원인이 관찰되지 않았을 가능성, 그리고 주변의 심한 기질성 섬유화 때문에 조영 증강 영상검사에서 병변이 노출되지 않았을 것으로 추정된다. 이와 같이 췌장의 세로토닌 분비 신경내분비종양은 비특이적 임상양상과 함께 췌관 폐쇄를 일으킬 수 있으며 특히 본 증례에서처럼 매우 작은 크기인 경우 폐쇄 원인인 종양이 관찰되지 않을 수 있어 췌장 신경내분비종양 진단에 주의가 필요하다.
REFERENCES
1. Pilichowska M, Kimura N, Ouchi A, Lin H, Mizuno Y, Nagura H. Primary hepatic carcinoid and neuroendocrine carcinoma: clinicopathological and immunohistochemical study of five cases. Pathol Int 1999;49:318-324.   2. Rockall AG, Reznek RH. Imaging of neuroendocrine tumours (CT/MR/ US). Best Pract Res Clin Endocrinol Metab 2007;21:43-68.   3. Klimstra DS, Modlin IR, Adsay NV, et al. Pathology reporting of neuroendocrine tumors: application of the Delphic consensus process to the development of a minimum pathology data set. Am J Surg Pathol 2010;34:300-313.   5. Furukawa H, Mukai K, Kosuge T, et al. Nonfunctioning islet cell tumors of the pancreas: clinical, imaging and pathological aspects in 16 patients. Jpn J Clin Oncol 1998;28:255-261.   6. Yao JC, Hassan M, Phan A, et al. One hundred years after “carcinoid”: epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol 2008;26:3063-3072.   7. Ganetsky A, Bhatt V. Gastroenteropancreatic neuroendocrine tumors: update on therapeutics. Ann Pharmacother 2012;46:851-862.   8. Paulson EK, McDermott VG, Keogan MT, et al. Carcinoid metastases to the liver: role of triple-phase helical CT. Radiology 1998;206:143-150.   9. Bader TR, Semelka RC, Chiu VC, et al. MRI of carcinoid tumors: spectrum of appearances in the gastrointestinal tract and liver. J Magn Reson Imaging 2001;14:261-269.   10. Kazanjian KK, Reber HA, Hines OJ. Resection of pancreatic neuroendocrine tumors: results of 70 cases. Arch Surg 2006;141:765-770.   11. Modlin IM, Kidd M, Latich I, Zikusoka MN, Shapiro MD. Current status of gastrointestinal carcinoids. Gastroenterology 2005;128:1717-1751.   12. Modlin IM, Lye KD, K idd M. A 5 ‐decade analysis of 13,715 carcinoid tumors. Cancer 2003;97:934-959.   13. Cheema A, Weber J, Strosberg JR. Incidental detection of pancreatic neuroendocrine tumors: an analysis of incidence and outcomes. Ann Surg Oncol 2012;19:2932-2936.   14. Kawamoto S, Shi C, Hruban RH, et al. Small serotonin-producing neuroendocrine tumor of the pancreas associated with pancreatic duct obstruction. Am J Roentgenol 2011;197:W482-488.   15. Hamada Y, Nakayama Y, Maeshiro K, Ikeda T, Hayashi H, Iwasaki H. Two cases of primary carcinoid tumor of the pancreas associated with marked stenosis of the main pancreatic duct. Pancreas 2009;38:834-835.  
Fig. 1.
Magnetic resonance cholangiopacreatographic (MRCP) finding. (A) Diffuse dilatation and localized stricture is observed on the main pancreatic duct. (B) MRCP shows atrophic parenchyma of the body and tail and focal nodule in pancreatic tail. 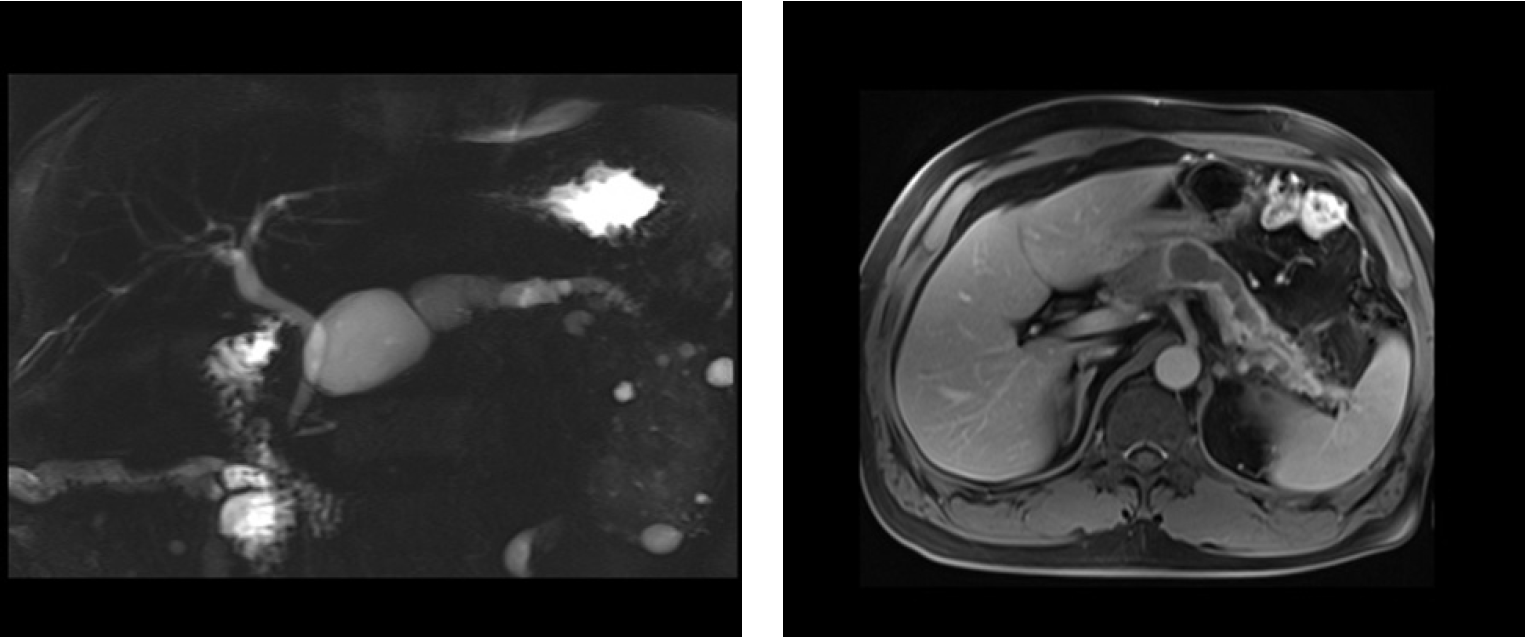
Fig. 2.
(A) Endoscopic ultrasonographic finding. A nodular lesion was identified in the dilated duct of pancreatic tail. (B) Gross specimen finding of pylorus-preserving pancreatoduodenectomy and splenectomy. Marked dilated pancreatic duct was exposed like a tumor. 
Fig. 3.
Microscopic findings for neuroendocrine tumors. (A) A small mass compressing pancreatic duct (white arrow) on the end of dilated duct (H&E, ×10). (B) Stromal fibrosis is shown around dilated pancreatic duct (H&E, ×40). (C) The ductal epithelium is intact without dysplasia. (H&E, ×100) (D) Tumor cell shows small round nuclei with abundant cytoplasm (H&E, ×400). 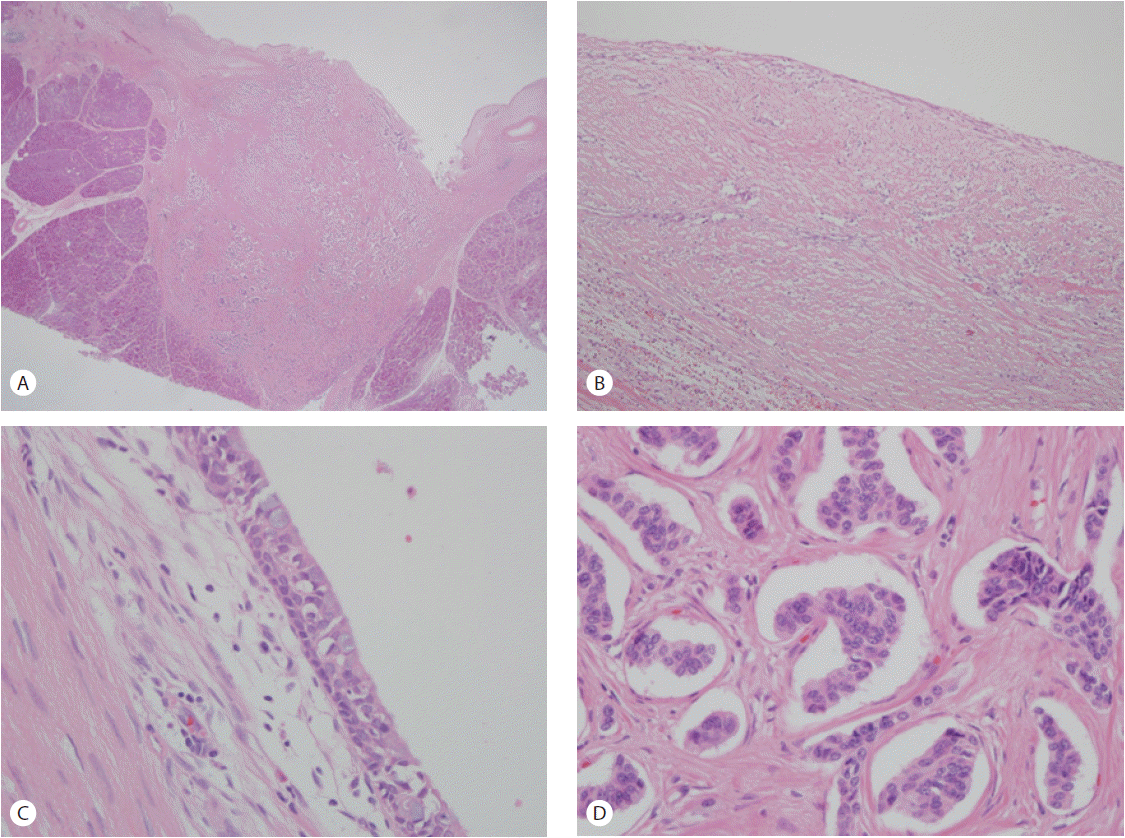
Fig. 4.
Positive immunohistochemical staining for CD56(A), synaptophysin(B), chromogranin(C), and Serotonin(D) (×400). 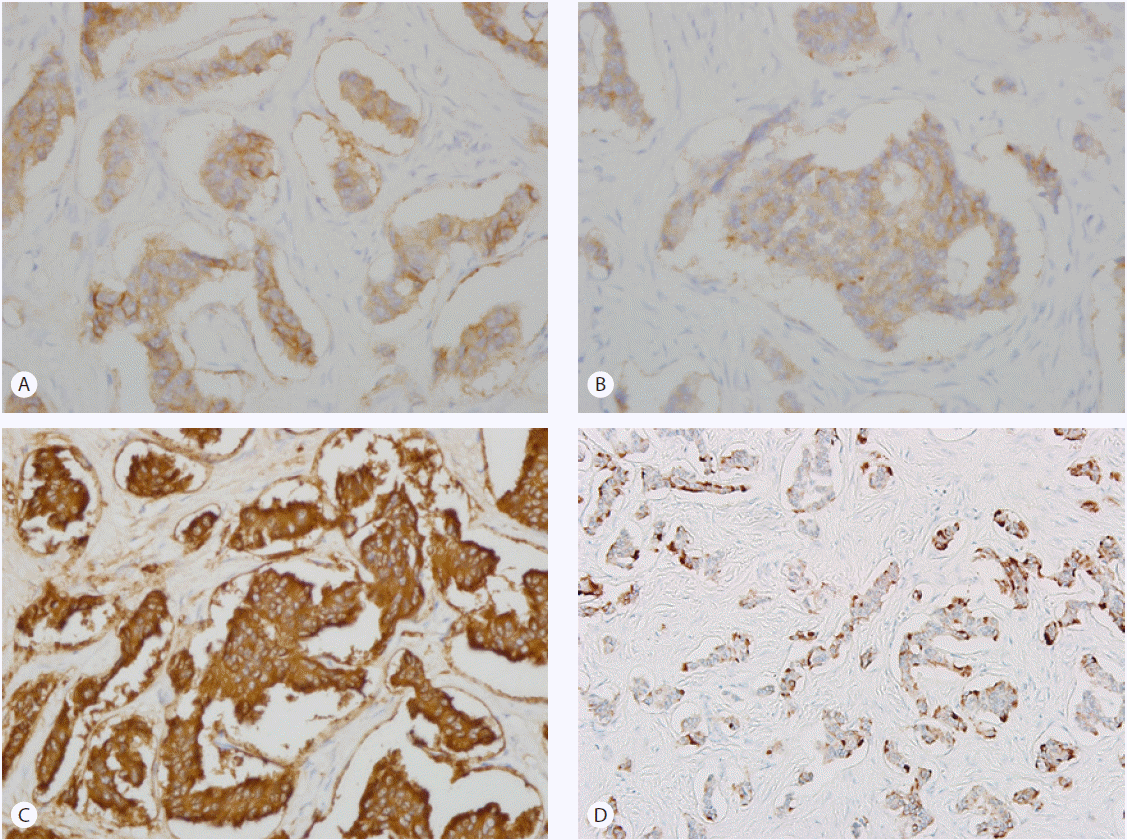
|
|
















