서 론
호산구성 담낭염은 Albot 등[1]이 1949년 처음 보고한 후 전체 담낭염의 0.25-6.4%를 차지하는 비교적 드문 질환으로, 담낭벽의 전층을 침윤한 염증세포 중 호산구가 90% 이상인 경우로 진단된다. 다른 일반적인 원인의 담낭염과 비교하여 증상, 검사실 소견 및 신체 검사에 있어 차이가 없어 주로는 담낭 절제술 후 진단하게 되며 이때 호산구성 담관염이 동반되는 경우가 극히 드물게 보고된다. 발병 기전은 명확하지 않으나, 담석 및 담관석 혹은 기생충 감염 등과 같은 만성 염증성 자극에 대한 과민반응, 과호산구증후군의 일부 형태 등이 원인으로 알려져 있다[2].
호산구성 방광염 또한 호산구성 담낭담관염과 마찬가지로 매우 드문 질환으로, Brown 등[3]이 1960년 처음 보고하였으며 방광벽의 전 층에 걸친 호산구 침윤으로 진단된다. 호산구성 방광염은 비특이적인 하부 요로 증상을 호소하여 주로 방광경을 통한 조직학적 진단을 통해서 진단되며, 재발이 잦다. 호산구성 위장관염에 호산구성 방광염이 동반된 증례들이 보고된 바 있으나[4], 호산구성 담낭담관염과 호산구성 방광염이 병발된 증례는 국외에서도 Mallat 등[5]이 2013년 보고한 1예만이 있으며 국내에서는 아직까지 보고된 바 없다.
한편, 최소 한 달의 간격을 두고 반복한 검사에서 말초혈액호산구 수치가 1,500/mm3 이상이거나, 병리학적으로 확인된 조직의 호산구 침범 및 이로 인한 기관의 손상 또는 기능이상이 있으면서, 이러한 손상 및 기능이상을 설명할 다른 요인이 없을 경우 과호산구증가증후군이라 한다[6]. 주로는, 피부, 폐, 위장관을 침범한다고 알려져 있으며, 췌담도계 및 비뇨계의 침범은 매우 드물다[7,8].
본 저자들은 심한 우상복부 통증을 동반한 무결석 급성담낭담관염으로 복강경하 담낭절제술 시행 후 호산구성담낭담관염이 진단된 환자에서 수술 후에도 지속된 호산구증가증과 심한 우상복부 통증 및 하부 요로 증상으로 경요로방광조직검사 후 호산구성 방광염이 확인되어 과호산구증가증후군 진단하에 경구 스테로이드 투약을 통해 증상 및 말초혈액 호산구증가증이 호전된 증례를 경험하였기에 보고하는 바이다.
증 례
49세 여자가 내원 3일 전부터 심해진 심와부 및 우상복부통증으로 내원하였다. 환자는 내원 1주 전부터 배뇨통 및 빈뇨로 급성 방광염 진단 하에 타 병원에서 경구 항생제(levofloxacin) 복용 중이었다. 20년 전 및 17년 전 총 2차례의 제왕절개술, 6년 전 및 1년 전 요로결석으로 2차례의 요로쇄석술, 3년 전 긴장성 요실금으로 수술한 기왕력 있었으나, 이 외에 특이할 만한 내과적 병력 및 가족력은 없었다. 내원 시 혈압은 132/84 mmHg, 맥박수는 90회/분, 호흡수는 20회/분, 체온은 36.6°C였고, 급성 병색을 보였으나 의식은 명료하였다. 복부 진찰에서 장음은 감소되어 있었으며, 심와부 및 우상복부의 압통은 있었으나 반발통은 없었으며, Murphy 징후도 관찰되었다.
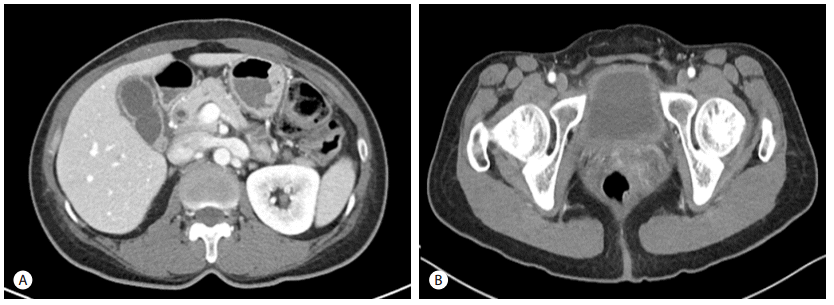
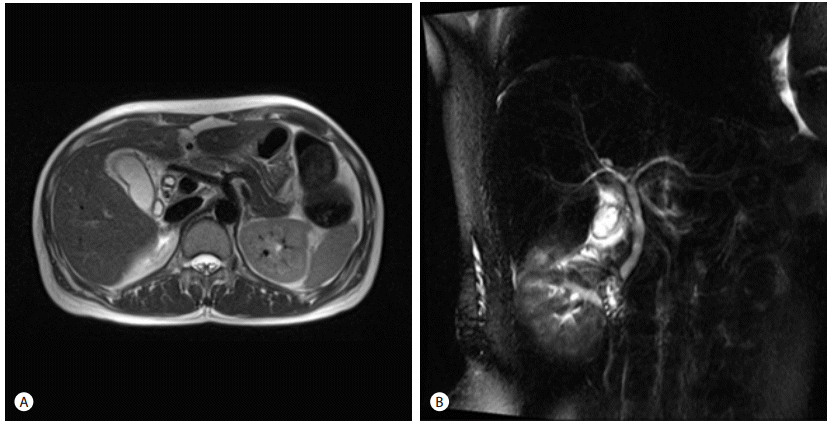
말초혈액검사에서 백혈구 6,900/µL (호중구: 72.3%, 4,960/mm3 호산구: 9.1%, 620/mm3), 혈색소 13.1 g/dL, 혈 소판 233,000/µL로 호산구는 경미하게 상승되어 있었으며, C-반응단백(C-Reactive Protein) 7.5 mg/L (정상범위, 0.1-5.0 mg/L) 역시 경미하게 상승되어 있었다. 아스파르테이 트 아미노전이효소 58 IU/L (정상범위, 5-40 IU/L), 알라닌 아미노전이효소 56 IU/L (정상범위, 5-40 IU/L), 총 빌리루 빈 0.3 mg/dL (정상범위, 0.2-1.4 mg/d), 알칼라인 포스파타 아제 76 IU/L (정상범위, 40-129 IU/L), 감마 글루타밀전이 효소 32 IU/L (정상범위, 8-69 IU/L)로 모두 정상 범위 이내 였다. 입원 2일째 시행한 혈청 총 IgE 항체는 97 (정상범위, 0-100 IU/mL)이었으며, 기생충 감염에 대한 혈청 특이 항체 검사 모두 음성이었다. 요검사에서 단백 1 (+), WBC 100 이상/HPF, RBC 100 이상/HPF였고, 심전도, 단순 흉부 및 복부 촬영에서 특이소견은 관찰되지 않았다. 복부전산 화 단층촬영에서 담낭벽의 비후와 조영증강 및 담낭 확장, 총간관에서 근위부 총담관에 걸친 담관벽 비후와 확장이 관찰되었으며(Fig. 1A) 방광벽도 비후되어 있었다(Fig. 1B). 복부 자기공명 담췌관조영술에서도 총담관의 확장은 있으나 내부의 담석은 관찰되지 않았다(Fig. 2A, B). 내시경 초음파에서 담관 주위의 폐쇄성 병변은 없었으며, 담낭석 및 담관석도 관찰되지 않았으나, 총담관의 미만성 비후 소견이 관찰되었다(Fig. 3A, B).
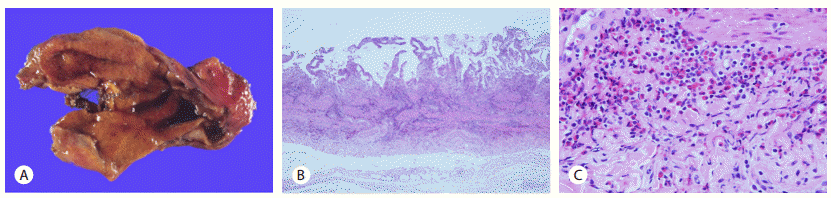
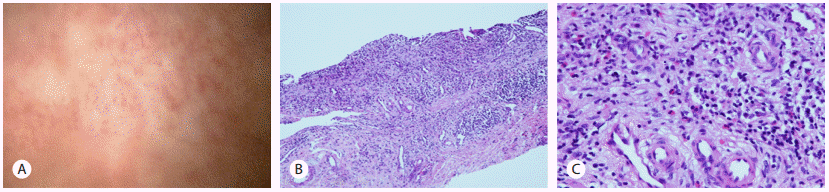
입원 직후 급성 담낭담관염 및 그에 동반된 방광염에 대해 경험적 항생제 치료(ciprofloxacin 400 mg 하루 2회, metronidazole 하루 3회 정주)를 시작하였으나 입원 2일째 38.3°C로 발열이 발생하며 우상복부 통증이 지속되는 경과를 보여 무결석 급성 담낭담관염 진단 하에 입원 5일째 복강경하 담낭절제술을 시행하였다. 절제된 담낭의 크기는 6.8×4.7 cm였고 내부에 담석은 발견되지 않았으며, 담낭벽의 두께는 0.5 cm였다(Fig. 4A). 저배율에서 담낭의 점막, 근육층 및 근육하 결합조직에까지 전층이 염증세포들로 침윤되어 있었다(Fig. 4B). 고배율에서는 염증세포의 90% 이상이 호산구로서, 고배율 당 약 234개의 호산구가 관찰되었다(Fig. 4C). 수술 후 우상복부 통증이 호전되어 경구 식이가 가능하였으나, 빈뇨, 잔뇨감 및 배뇨통 등 급성요로증상은 지속되었다. 요배양, 요세포검사에서는 특이 소견 없었으나, 지속되는 급성요로증상으로 담낭 절제술 후 20일째 시행한 방광경 검사에서 방광 점막의 홍반성 변화가 관찰되어 경요로방광생검을 시행하였다. 생검한 조직의 크기는 약 0.3 cm였으며, 방광 조직에서는 염증세포들의 침윤이 관찰되었고, 대부분의 세포들은 림프구였으며 염증세포의 약 20%가 호산구로서 고배율 당 14개의 호산구가 관찰되었다(Fig. 5B). 경구항생제와 수액치료를 유지하였음에도 증상이 지속되며 말초 혈액 호산구 수치가 1,200/mm3으로 상승하는 경과(Fig. 6)를 보여 호산구성 방광염의 가능성이 임상적으로 강력히 의심되어 경구 prednisolone 30 mg 하루 1회(0.75 mg/kg) 투약을 경요로방광생검 2일 전 이미 시작한 상태였다. 최종적으로 담낭벽과 방광벽에서 각각 시행한 조직생검 결과 상기 호산구 침윤이 확인됨에 따라 과호산구증가증후군 진단 하에 경구 prednisolone 투약을 유지하며 급성요로증상은 호전되는 경과를 보였으며, 말초혈액의 호산구도 정상 범위 이내로 감소하였다. 상기 용량으로 2주간 유지 후 감량하여 10 mg 하루 1회로 총 1개월간 유지 후 중단하였으며 외래에서 추적 관찰하였을 때 증상의 재발은 없었다. 아울러 진단 시 경도의 총담관벽의 비후 소견에 대해 3개월째 외래에서 시행한 내시경 초음파에서 담관벽의 비후가 호전되었음을 확인하였다.
고 찰
호산구성 담낭염은 Albot 등[1]이 1949년 처음 보고하였으며, 호산구성 담관염은 Leegard 등[9]이 1980년 처음 보고한 이례로 비교적 드물게 보고되고 있다. 이러한 호산구성 담낭염은 말초 호산구증가증의 동반 여부와 상관없이, 조직 또는 기관의 호산구 침윤을 특징으로 하는 광범위한 질환의 하나이다. 그렇기에 그 원인으로써 기왕에 존재하던 담석 또는 담즙에 대한 국소적인 알레르기 반응에서부터 기생충을 포함하는 감염, 알레르기, 약제, 생약(herbal medication), 호산구성 위장관염, 과호산구증후군 및 호산구-통증 증후군(eosinophilia-myalgia syndrome) 등에 의한 이차적인 반응까지 다양한 원인이 작용할 수 있음이 알려져 있다. 또한 결석성 담낭염보다 무결석 담낭염에서 보다 잘 발생하는 것으로 알려져 있다[2,10].
일반적인 담낭염과는 증상 및 검사실 소견으로 구분되지 않으므로 주로 담낭절제술 후 진단되는 경우가 대부분이다. 외국의 사례에서는 Fox 등[11]이 영국에서 625건의 담낭절제술 중 16건에서 호산구 침윤을 확인하였다. 국내에서는 염 등이 3,539건의 담낭절제술 중 30건에서 호산구 침윤을 확인하였으며, 이 중 6건에서 말초혈액호산구 증가가 동반되어 있었다[12]. 따라서 말초혈액호산구 증가가 호산구성 담낭염의 중요한 예측 인자로 주장되었으나, 앞서 언급한 것처럼 호산구증의 동반은 호산구성 담낭염의 진단에 필수적이지는 않다. 그러나 조직학적으로 확인된 담낭벽의 호산구 침윤 및 침윤 정도는 진단에 절대적이며, 호산구 침윤정도가 50-75%일 경우에는 림프-호산구성 담낭염(lympho-eosinophilic cholecystitis), 90% 이상일 경우에 호산구성 담낭염(eosinophilic cholecystitis)으로 진단하게 된다. 이러한 호산구 침윤과 관련하여, 호산구성 담낭염은 아니나, 기존에 연구된 호산구성 위장관염에서는 IL-3, GM-CSF, IL-5와 같은 cytokine을 통해 호산구의 침윤 및 호산구전 세포(eosinophil precursor)의 호산구로의 분화 및 증식을 촉진하는 것으로 알려져 있다[13]. 호산구성 담낭염 역시 이러한 분자생물학적 기전과 연관되어 있을 가능성이 높으나, 이와 관련한 정확한 분자생물학적 기전의 규명이 필요하다.
호산구성 방광염은 Brown [3]이 1960년 처음 보고하였으며, 방광벽의 전층에 걸친 호산구 침윤으로 진단된다고 알려져 왔으나, 급성과 만성등 경과에 따라 호산구 침윤이 다르며, 고배율에서는 고배율당 1개 이상의 호산구가 관찰되어도 호산구성 방광염으로 진단한다[14]. 본 증례에서는 호산구성 담낭염이 이미 진단된 상태에서 요로 증상의 지속과 호산구 수치의 상승을 보여 임상적으로 호산구성 방광염이 강하게 의심되는 상태에서 치료를 주저할 수 없어 스테로이드 투약을 시작하였고, 투약 3일째 경요로방광생검을 시행하였기에, 담낭에 비해서 호산구의 침윤정도가 방광벽에서 낮게 나왔을 것으로 생각된다. 스테로이드 투약 전 경요로방광생검이 이루어졌다면 바람직하였겠으나, 호산구성 방광염의 진단 자체에는 무리가 없는 결과를 보였다. 한편, 호산구성 방광염은 호산구성 담낭염과 마찬가지로 기생충 감염, 호산구성 위장관염, 약제 등의 원인 외에 반복되는 요로감염, 만성 육아종성 질환, 방광 내 mitomyin C 주입, 경요도전립선절제술(transurethral resection of the prostate, TURP)과 같은 비뇨기 처치도 가능한 원인으로 알려져 있다. 그러나 이 역시 빈뇨, 배뇨통, 혈뇨 등과 같은 비특이적인 하부 요로 증상을 나타내므로 임상적으로 진단하기 어려우며, 조직학적 진단을 통해서 확진한다. 외국에서는 Van den Ouden 등[15]이 135개의 호산구성 방광염으로 진단된 기존 증례들을 분석한 결과, 43%에서 말초혈액 호산구 증가가 있었으며, 50%의 환자에서는 아토피 또는 알레르기의 기왕력이 있음을 확인할 수 있었다. 그러나 말초혈액 호산구증가증의 동반 여부 혹은 증가 정도와 질환의 예후와의 관련성 등에 대해서는 밝혀진 바 없다.
본 증례처럼 호산구성 담낭염과 호산구성 방광염이 병발된 증례는 국외에서도 Mallat 등[5]이 2013년 보고한 1예만이 있으며, 국내에서는 현재까지 보고된 바가 없다. Mallat 등[5]은 연관성이 낮은 독립된 장기에 우연히 병발한 증례로 접근하였으나, 본 저자들은 말초혈액 호산구증가증을 동반하며 연관성이 낮은 독립된 장기의 염증을 일으켰다는 점에 비추어 전신질환인 과호산구증가증후군의 가능성으로 본 증례를 접근하는 것이 바람직하다고 보았다. 과호산구 증가증후군의 진단 기준은, 6개월 이상 지속되는 1,500/mm3 이상의 말초혈액호산구 수치에서, 2012년 개정안에서는 명확한 유발 요소가 없는 상태에서 최소 한 달의 간격을 두고 반복한 검사에서 말초혈액호산구 수치가 1,500/mm3 이상이거나 병리학적으로 확인된 조직의 호산구 침범 및 이로 인한 기관의 손상 또는 기능이상이 있으면서, 이러한 기관의 손상 및 기능이상을 설명할 다른 요인이 없을 경우로 수정되었다[6]. 본 환자는 알레르기 기왕력, 증상 발생에 선행한 약물 복용력, 최근의 여행력 및 동물 생식력이 없었으며 기생충 관련 검사에서도 유의한 소견이 관찰되지 않았다. 이에 본 환자의 호산구성 담낭염 및 방광염은 과호산구증가증후군의 일환으로 볼 수 있으며, 이차성 원인이 배제된 500-1,500/mm3 의 경도의 호산구증가증에 대해서는 골수 검사 없이 경과 관찰할 것을 권고하고 있으므로[16], 향후 경과 관찰에 따라 추가적인 진단 및 치료방침을 수립을 고려해 볼 수 있다. 또한 환자는 스테로이드 치료 이후 외래 추적 관찰에서도 말초혈액 호산구증가 및 말초혈액 도말검사의 이상 없이 양호한 경과를 유지하고 있어서 당장의 골수검사는 필요없을 것으로 사료된다.
주요 장기의 기능이상을 동반하지 않는 무증상의 과호산구증가증후군의 치료에 대해서는 일관된 견해가 없으나, 증상이 있는 과호산구증가증후군에서는 전신 스테로이드제가 일차적인 선택 약제로 알려져 있으며, 스테로이드 치료에도 호전이 없을 경우 hydroxyurea, vincristine, alkylating agent, cyclosporine, etoposide 등을 고려해 볼 수 있다[17]. 그러나 본 증례에서는, 내원 시 말초혈액호산구 600/mm3로 경도로 상승된 상태에서 우상복부통증과 발열이 지속되는 급성 담낭염의 경과를 보였기에, 호산구성 담낭염 단독보다는 무결석 담낭염 및 추후 확인되어야 할 다른 호산구 상승의 원인들이 독립적으로 존재할 것으로 생각하여 급성기 치료인 담낭절제술을 우선적으로 시행하였다. 이후 담낭 절제술을 통한 담낭 조직 검사에서 담낭벽의 호산구 침윤 소견이 관찰되어 호산구성 담낭염이 확인되었으며, 수술 후 복부 증상이 소실된 상태에서 급성 요로 증상과 말초 혈액 호산구의 경도 상승이 다시 발생하여 호산구성 방광염의 가능성을 의심하여, 이 시점에서 경구 스테로이드제 투약을 시작하였다. 호산구성 담낭염에서는 상기 진단이 의심되어 스테로이드 투약을 통해 호전되어 수술적 치료를 시행하지 않은 증례가 보고되었으나[18], 대부분의 진단이 수술 후 조직검사를 통해 후향적으로 내려지므로 초치료 및 추후 추적 관찰에 대한 명확한 가이드라인이 제시되어 있지 않은 것이 현실이다.
그러나 방광절제술의 시행은 쉬운 선택이 아니기에, 호산구성 방광염에 있어서는 스테로이드제 투약 후 재발 시 면역억제제(cyclosporine/azathioprine)를 사용하고, 이후에도 심한 혈뇨 및 신기능 저하 등이 관찰될 경우 방광절제술을 시행할 것을 고려하도록 되어 있다[19]. 과호산구증가증후군의 일환으로서 개개의 치료에 접근하면 무리가 없을 것으로 사료되나, 특히 호산구성 담낭염에서의 초치료로서 수술적 및 내과적 치료의 예후 및 재발에 대한 광범위한 비교 연구(head-to-head study)가 요하며 내과적 치료에 대한 구체화된 가이드라인의 확립이 필요할 것으로 보인다.