간농양과 감별이 어려웠던 간내 육종양 담관암 1예
요약
간내 육종양 담관암은 간내 담관암의 비교적 드문 변이형으로 간내 증식 및 전이 혈관 침범 등이 흔해 예후가 불량하다고 알려져 있다. 따라서 완치를 위해서는 조기진단과 적극적인 치료가 무엇보다 중요하다. 본 저자들은 영상학적 검사와 간생검을 하였지만 임상 진단이 불충분하였던 간 병변을 수술 후 병리조직검사를 통해 간내 육종양 담관암으로 확진한 증례를 경험하였기에 보고한다. 기존에 보고되었던 증례들과 달리, 초기 병기로 확인되어 비교적 좋은 예후가 기대되는 바이다.
Keywords: 담관암, 육종양, 간농양
Abstract
Sarcomatoid transformation of intrahepatic cholangiocarcinoma is rarely found but usually has very poor prognosis due to the lack of effective approaches for early detection and its aggressive nature. We report a case of this tumor type, in a 60-year-old man who was referred to our hospital for further evaluation of screening-detected, asymptomatic hepatic lesion. Clinical diagnosis was elusive despite performance of different imaging modalities and a transcutaneous liver biopsy. Pathology of the surgically resected tumor demonstrated intrahepatic sarcomatoid cholangiocarcinoma. In our case, tumor cells expressed strong immunoreactivity to both cytokeratin-19 and vimentin. We assume the relatively good prognosis of this patient would be expected because surgery played a critical role at an early stage of the tumor.
Keywords: Cholangiocarcinoma, Sarcomatoid, Spindle cell, Cytokeratin, Vimentin
서 론
간내 담관암은 간세포암에 이어 두번째로 흔한 원발성 간암으로 전체 원발성 간암의 약 10-15%정도를 차지하며 조직학적으로는 대부분이 선암이다[ 1]. 미분화암의 일종인 육종양 암종은 간내 담관암 중 비교적 드문 변이형으로, 담관암 부검 증례에서 약 4.5%의 빈도로 관찰된다고 보고된 바 있다[ 2]. 간내 육종양 담관암(intrahepatic sarcomatoid cholangiocarcinoma)은 간담도에 발생하는 암들 중 예후가 불량한 것으로 알려져 있으며, 이는 육종성 요소로 인해 간내 증식 및 전이 혈관 침범이 비교적 흔하기 때문이다[ 3, 4]. 따라서 완치를 위해서는 이른 병기에서의 진단이 무엇보다 중요하다. 하지만, 조직학적 진단을 위해서는 면역조직화학 염색상 선암종 부위와 함께 다형성 방추형 종양 세포가 확인되어야 하는데, 육종양 암종은 광범위한 괴사를 동반하는 것을 특징으로 하기 때문에 많은 양의 검체를 얻기가 쉽지 않은 경피적 간생검으로는 진단이 불충분할 수 있고, 영상학적 진단에도 제한이 있어 수술 전까지는 확진이 어려운 경우가 많다[ 5]. 이에 저자들은 간농양으로 임상 진단하였으나 수술 후 병리조직검사를 통해 초기 병기의 간내 육종양 담관암으로 진단한 증례를 경험하였기에 문헌고찰과 함께 이를 보고하는 바이다.
증 례
60세 남자가 타 병원에서 검진 목적으로 시행한 복부초음파에서 장경 3.0 cm 정도의 종괴가 발견되어 복부 전산화단층촬영(computed tomography, CT) 시행 후 간내 농양 의심되어 본원으로 전원되었다. 내원 6개월 전 당뇨를 진단받아 약을 복용 중이었으며, 그 외 특이 병력은 없었다. 내원 당시 혈압 120/80 mmHg, 체온 36.4℃, 맥박수 74회/분, 호흡수 20회/분이었다. 흡연력 및 음주력은 없었으며, 가족력에서 특이사항은 없었다. 전신 쇠약감 및 체중감소는 없었으며, 발열, 오한, 구토, 복통 등의 증상도 없었다. 공막에 황달은 보이지 않았고, 복부는 부드럽고 편평하였으며, 우상복부 촉진에서 압통은 없었고 종괴도 명백하게 촉지되지 않았다. 말초혈액검사에서 백혈구 5,000/mm 3, 혈색소 14.2 g/dL, 혈소판 182,000/mm 3 였고 C- 반응단백 5 mg/dL 미만이었다. 혈청생화학검사에서 아스파르테이트아미노전달효소(AST) 34 IU/L, 알라닌아미노전달효소(ALT) 42 IU/L, 총 빌리루빈(total bilirubin) 1.0 mg/dL, 알칼리성인산염분해효소(ALP) 55 IU/L, 혈중요소질소(BUN) 16.5 mg/dL, 크레아티닌 0.73 mg/dL였다. 바이러스 혈청검사에서 B형 간염 바이러스 표면 항원 및 C형 간염 바이러스 항체는 음성이었다. 혈청 종양표지자검사에서 알파태아단백(AFP), proteins induced by vitamin K absence or antagonist-II (PIVKA-II)는 각각 2.93 ng/mL, 18 mAU/mL 으로 정상 범위였으나 cabohydrate antigen 19-9 (CA 19-9)는 84.06 U/mL로 증가되어 있었다. 외부 병원에서 시행한 CT 사진( Fig. 1)과 본원 내원하여 시행한 자기공명영상(magnetic resonance imaging, MRI) 사진( Fig. 1)에서 간의 우엽 제8구역의 문맥기와 지연기 모두에서 변연 부위가 조영 증강 소견을 보이는 약 3 cm 크기의 타원형 종괴가 확인되었다. 병변의 내부는 격막을 보이는 저음영의 낭성 종양 형태를 띠고 있었으며 MRI상 T1강조영상에서 낮은 신호 강도를 보이고 T2강조영상에서 높은 신호 강도를 보이는 등 영상학적 소견으로는 간농양이 우선적으로 의심되었다. 하지만 간내 담관암 역시 배제할 수 없었다. 양전자방출 컴퓨터단층촬영(positron emission tomography/CT, FDG-PET/CT)에서는 간의 8번 구역 부위에 종괴 양상의 음영은 확인되었으나 명확한 FDG 섭취 증가 소견은 관찰되지 않았다. 병리조직학적 확인을 위해 입원 후, CT 유도하 경피적 간 조직검사를 시행하여 2개의 조직을 얻었으나 담관의 경도 이형성 변화(mild dysplastic changes)와 담관 주위 염증 및 섬유화를 보일 뿐 악성 세포는 관찰되지 않았다( Fig. 2). 간문맥기 조영증강 CT에서 변연부에 조영증강이 있으면서 중심부는 저감쇠(hypoattenuating) 병변으로 관찰되었으며 주변 간내 담도의 확장 등도 동반하지 않아 영상학적으로는 간농양이 의심되었다. 시행한 경피적 간 조직검사에서도 악성 세포가 보이지 않았지만 간농양 등의 간의 염증성 병변과는 달리 압통이나 발열 등 감염의 증거가 없고, CA 19-9 상승 소견 등을 참고할 때 간내 담관암 등의 악성 종양을 배제할 수 없어 수술적 진단과 치료를 위해 외과와 협진하였고 간의 8번 구역절제술을 시행하였다. 수술 조직의 육안소견에서 종양은 3.0 × 2.5 × 2.5 cm으로 측정되었으며, 현미경 소견에서 고도로 분화된 선암종(well differentiated adenocarcinoma), 방추 세포(spindle cell)가 확인되며 알파태아단백 등의 간세포 표지자는 음성이었다. 유사분열지수(mitosis)의 정도는 10 HPF (high power field) 중 1 mitosis 이하였고 경도에서 중등도의 다형성(pleomorphism) 소견을 보였다. 혈관-림프관 침윤(angiolymphatic invasion)이나 주변 임파선전이는 없었다. 절제면의 암세포는 음성 소견을 보여 암종의 완전 절제가 확인되었다. 면역조직화학 검사에서 cytokeratin-19 (CK-19)과 vimentin 양성 소견이 확인되어 간내 육종양 담관암으로 진단할 수 있었다( Fig. 3). 수술 후 최종 병기는 7판 AJCC TNM 병기 분류법[ 6]에 따라T1N0M0로 확인되었다. 환자는 수술 후 12일째 안정적인 경과를 보여 퇴원하였으며, 현재 외래에서 4개월째, 복부 CT에서의 재발소견이나 종양 표지자의 상승 없이 추적관찰 중이다.
고 찰
육종양 암종은 방추세포암(spindle cell carcinoma)이나 가육종(pseudosarcoma) 등으로 불리우는데 이러한 상피암종의 육종형 변화는 폐, 식도, 피부 등과 같이 편평상피가 분포하는 곳에서 주로 발생하나 신장, 유방, 위 등에서 발생한 예가 드물게 보고되고 있다[ 7, 8]. 원발성 간암에서의 육종양 변화는 간세포암에서 가장 흔하며, 특히 항암치료나 경동맥 화학 색전술(transarterial chemoembolization, TACE) 후에 잘 관찰된다[ 9]. 하지만, 간내 담관의 육종양 변화는 간세포암에 비해 드물며 항암치료와의 연관성도 알려진 바가 없고 발병 기전도 명확하게 밝혀지지 않았다. Yoo 등[ 10]은 유전학적 형질 발현에 의한 담관 상피세포의 미분화 시기에 육종양 세포로의 변화 가능성을 병인 중 하나로 제시하기도 하였다. 간내 육종양 담관암과 일반적인 간내 담관암을 조직학적 확진 전에 미리 구별하는 것은 매우 어렵다. 일반적인 간내 담관암은 우상복부 동통이나 황달 등의 다양한 증상을 주소로 내원하게 되며 조직학적으로는 잘 분화된 선암종이 대부분을 차지한다. 혈청 CA 19-9는 85% 이상에서 증가한다고 알려져 있으며 항암화학요법이나 방사선치료에 잘 듣지 않는 경우가 흔해 전반적인 예후는 불량하지만 병의 진행 속도는 느릴 수 있다. 에에 반해 간내 육종양 담관암은 일반적인 간내 담관암에서 보이는 우상복부 동통, 황달 등의 일반적인 증상에 비해 열감을 자주 호소하고 CA 19-9 등의 종양 표지자가 음성인 경우가 많으며 조직학적으로 대부분에서 중증도 혹은 분화가 나쁜 선암 세포 및 방추 세포 등의 다양한 세포들이 혼합된 형태를 보인다[ 11- 13]. CT 검사에서 변연부 조영을 동반한 저음영 병변이 보이고 MRI 영상에서 T1강조영상에서는 등신호 혹은 저신호 강도를 보이며, T2 강조영상에서는 고신호와 저신호 강도가 혼재되어 있는 비균질 종괴 형태가 특징적인 영상학적 소견이라는 보고도 있으나 이것만으로 진단하는 것은 쉽지 않다. 따라서 면역조직화학검사가 정확한 진단을 위해 필수적이다. 본 증례의 환자는 발열 증상이 없었으며 CA 19-9 가 상승된 소견을 보여 앞에서 언급된 간내 육종양 담관암의 특징적인 소견과는 달랐다. 또한 본 증례의 환자는 외부 병원에서 복부 CT 촬영 후 간농양이 의심되어 의뢰되었는데 임상적으로 우상복부 동통, 발열, 오심 등의 증상은 간농양에서, 식욕부진, 피로감, 무통성 황달, 체중감소 등은 간내 담관암에서 각각 흔하다고 알려져 있으나 간농양과 간내 담관암을 구분 짓는 특징적인 증상은 아니다. 복부 초음파검사에서 간농양은 주로 저음영 변병으로 나타나고 변연은 불규칙하며 내부에 격막이나 공기음영(gas bubbles) 등을 포함할 수 있다. 동맥 강조기 CT에서 간농양은 3개의 층을 보이는데 중심부 괴사부위는 저음영이고, 다음 바깥 층은 환상 조영되는 고음영의 띠로, 섬유성 조직이 풍부한 가장 바깥 층은 저음영으로 보여 이중 표적 징후(double target sign) 를 나타낸다. 이에 비해 복부 초음파에서 간내 담관암은 불규칙한 변연부와 위성 결절(satellite nodule) 을 보이는 고음영의 종괴로 주로 관찰되고 CT에서는 담관 확장을 동반한 저음영 종괴로 주로 나타난다. 역동적 CT 의 동맥기, 문맥기에서 종양세포가 풍부한 가장자리부는 조영증강 소견을 보이며, 섬유성 간질이 풍부한 중심부는 저음영을 나타난다. 평형기에서는 중심부가 지연성으로 조영되고 반대로 종괴의 변연부는 저음영을 보이는 것이 특징적이다. 또한 종괴가 간 피막에 침윤시, 간 표면에 함요(cancer navel) 를 동반하기도 한다. MRI 의 T1 강조영상에서는 주변의 정상 간질과 비교하여 저신호, T2강조영상에서는 등신호이거나 약한 고신호 강도를 보인다. 또한 T2강조영상에서 종괴의 중심부는 풍부한 섬유질을 반영하여 등신호 혹은 약한 저신호를 나타내며, 내부에 점액 분비물을 포함하고 있으면 중증도의 고신호를 보이고 한다. 병리학적으로, 상피세포의 분화에서 육종성 변화는 핵의 다형성이 동반된 방추 세포가 주로 판이나 다발 모양으로 배열되고 면역조직화학 염색에서 상피세포 표지자인 cytokeratin 과 간엽세포 표지자인 vimentin 양성을 보이는 것이 특징이라고 알려져 있다[ 7, 13]. 본 증례의 환자에서도 CK-19 와 vimentin 에 대한 면역조직화학 염색에 방추형 세포가 모두 양성 소견을 보여 간내 육종양 담관암으로 확진할 수 있었다. 아직 간내 육종성 담관암치료에 대하여 명백한 가이드라인은 없으며, 수술적 치료를 했을 때 하지 않은 환자들보다 유의하게 생존율이 높은 것 정도만 알려져 있다[ 12]. 수술 후 보조항암화학요법에서도 전이성 담관암과 육종에 반응이 있는 것으로 알려져 있는 젬시타빈(gemcitabine), 시스플라틴(cisplatin) 병용요법을 투여한 증례가 있을 뿐, 효과가 입증되지 않았다[ 14]. 따라서 간내 육종양 담관암의 기본 치료 원칙은 종괴의 수술적 절제이다. 간내 육종양 담관암은 원격전이가 흔하고 높은 침습성으로 인해 급격히 진행되어 일반적인 간내 담관암에 비해 나쁜 예후를 보이는 알려져 있는데, 현재까지 보고된 국내외 증례에서는 대부분 육종양 담관암 환자들이 진단 당시부터 진행된 병기를 보였고 이로 인해 적극적인 치료에도 불구하고 그 결과가 좋지 못하였다( Table 1)[ 8, 13, 15]. 이와 달리, 이번 증례에서는 수술 후 병기가 AJCC/UICC stage I로 확인될 정도로 이른 병기에서 완전 절제가 이루어져서 비교적 좋은 예후가 기대된다. 결론적으로, 간내 육종양 담관암은 비교적 드물고 일반적인 담관암과 구분 지을 수 있는 특징적인 임상학적 소견이 부족하여 병리조직검사 없이 미리 진단하는 것이 쉽지 않기 때문에 적극적으로 감별진단을 하려는 노력이 필요하다 . 특히 종양의 높은 침습성으로 인해 예후가 매우 좋지 않기 때문에, 조기 진단 및 치료가 무엇보다 중요하다 할 수 있겠다.
REFERENCES
1. Parkin DM, Ohshima H, Srivatanakul P, Vatanasapt V. Cholangiocarcinoma: epidemiology, mechanisms of carcinogenesis and prevention. Cancer Epidemiol Biomarkers Prev 1993;2:537-544.  2. Sato K, Murai H, Ueda Y, Katsuda S. Intrahepatic sarcomatoid cholangiocarcinoma of round cell variant: a case report and immunohistochemical studies. Virchows Arch 2006;449:585-590.  3. Watanabe G, Uchinami H, Yoshioka M, Nanjo H, Yamamoto Y. Prognosis analysis of sarcomatous intrahepatic cholangiocarcinoma from a review of the literature. Int J Clin Oncol 2014;19:490-496.   4. Aishima S, Kuroda Y, Asayama Y, et al. Prognostic impact of cholangiocellular and sarcomatous components in combined hepatocellular and cholangiocarcinoma. Hum Pathol 2006;37:283-291.   5. Kakizoe S, Kojiro M, Nakashima T. Hepatocellular carcinoma with sarcomatous change. Clinicopathologic and immunohistochemical studies of 14 autopsy cases. Cancer 1987;59:310-316.   6. Sobin LH, Compton CC. TNM seventh edition: what’s new, what’s changed: communication from the International Union Against Cancer and the American Joint Committee on Cancer. Cancer 2010;116:5336-5339.   7. Haratake J, Horie A. An immunohistochemical study of sarcomatoid liver carcinomas. Cancer 1991;68:93-97.   8. Wi JH, Ahn MS, Chung SO, et al. A case of sarcomatoid carcinoma in the gallbladder. Korean J Med 1999;57:1048-1052.
9. Kojiro M, Sugihara S, Kakizoe S, Nakashima O, Kiyomatsu K. Hepatocellular carcinoma with sarcomatous change: a special reference to the relationship with anticancer therapy. Cancer Chemother Pharmacol 1989;23(Suppl):4-8.  11. Shimada M, Takenaka K, Rikimaru T, et al. Characteristics of sarcomatous cholangiocarcinoma of the liver. Hepatogastroenterology 2000;47:956-961.  12. Kaibori M, Kawaguchi Y, Yokoigawa N, et al. Intrahepatic sarcomatoid cholangiocarcinoma. J Gastroenterol 2003;38:1097-1101.   13. Kim WS, Kim TH, Hwang JJ, et al. A case of intrahepatic sarcomatoid cholangiocarcinoma with rhabdoid transformation. Korean J Med 2011;80:453-457.
14. Malhotra S, Wood J, Mansy T, Singh R, Zaitoun A, Madhusudan S. Intrahepatic sarcomatoid cholangiocarcinoma. J Oncol 2010;2010:701476.  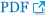
Fig. 1.
Selected images of this case from various preoperative image modalities. (A) Ultrasound image of a low-level echo collection with a relatively well-defined mass in the right lobe of the liver. (B) Portal venous-phase contrast-enhanced computed tomography (CT) scan showing approximately 3 × 2 cm of a heterogeneously low density lesion with peripheral enhancement on segment 8 of the right hepatic lobe. (C) Axial T-weighted magnetic resonance imaging (MRI) revealing a central aspect with high signal intensity and internal septa, which is surrounded by an inflamed area slightly hypointense to the liver. (D) Positron emission tomography/computed tomography (PET/CT) scan showing no definite FDG uptake in the position where the lesion was confirmed in other image modalities. 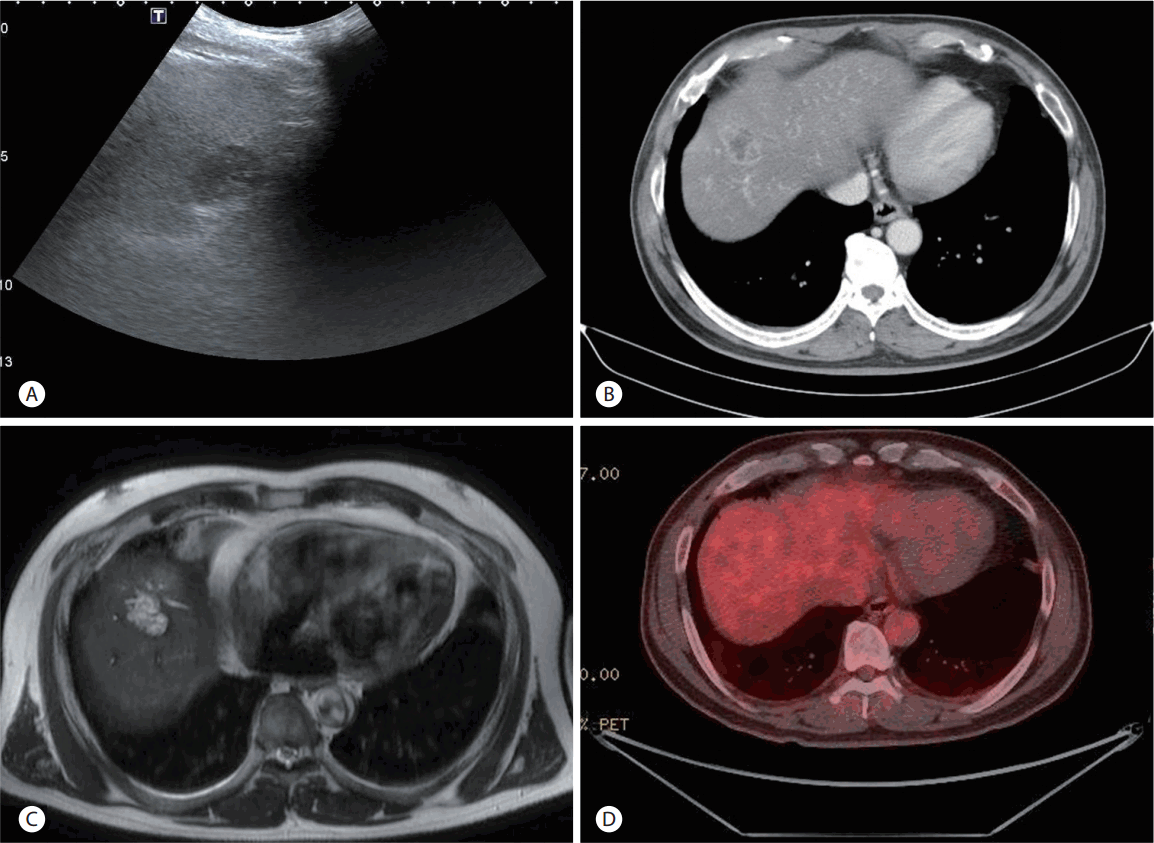
Fig. 2.
(A) Photomicrograph of percutaneous liver biopsy shows only a mild atypical epithelial proliferation without evidence of definite tumor cells (H&E, ×200). (B) Immunohistochemistry using pan-cytokeratin reveals reactivity with the epithelial component (pan-cytokeratin, ×200), but (C) negative for vimentin due to an absence of a sarcomatous component (vimentin, ×200). A liver biopsy failed to elucidate the diagnosis in this patient. 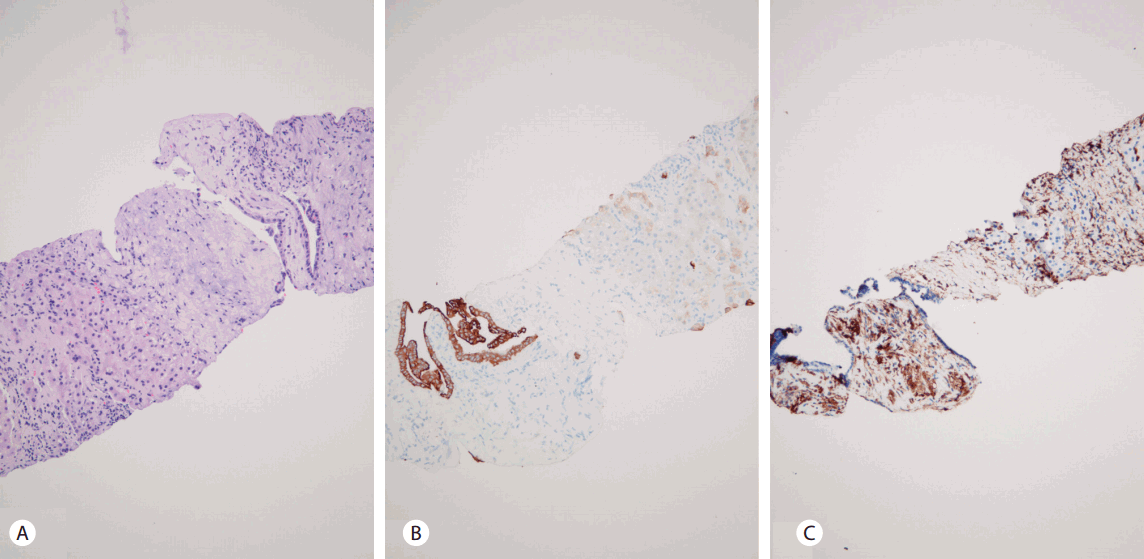
Fig. 3.
Microscopic findings from a resected specimen. (A) Tumor cells reveal a malignant biphasic neoplasm consisting of well differentiated carcinomatous and sarcomatous components with a loosely textured arrangement of spindle cells (H&E, ×40). (B) The glandular structures show moderate nuclear pleomorphisms with prominent nucleoli and frequent mitosis (H&E, ×200). (C) Immunohistochemistry with the antibody to cytokeratin-19 (CK-19) shows strong reactivity with the epithelial component (CK-19, ×200). (D) The tumor cells are strongly immunoreactive to vimentin (vimentin, ×200). 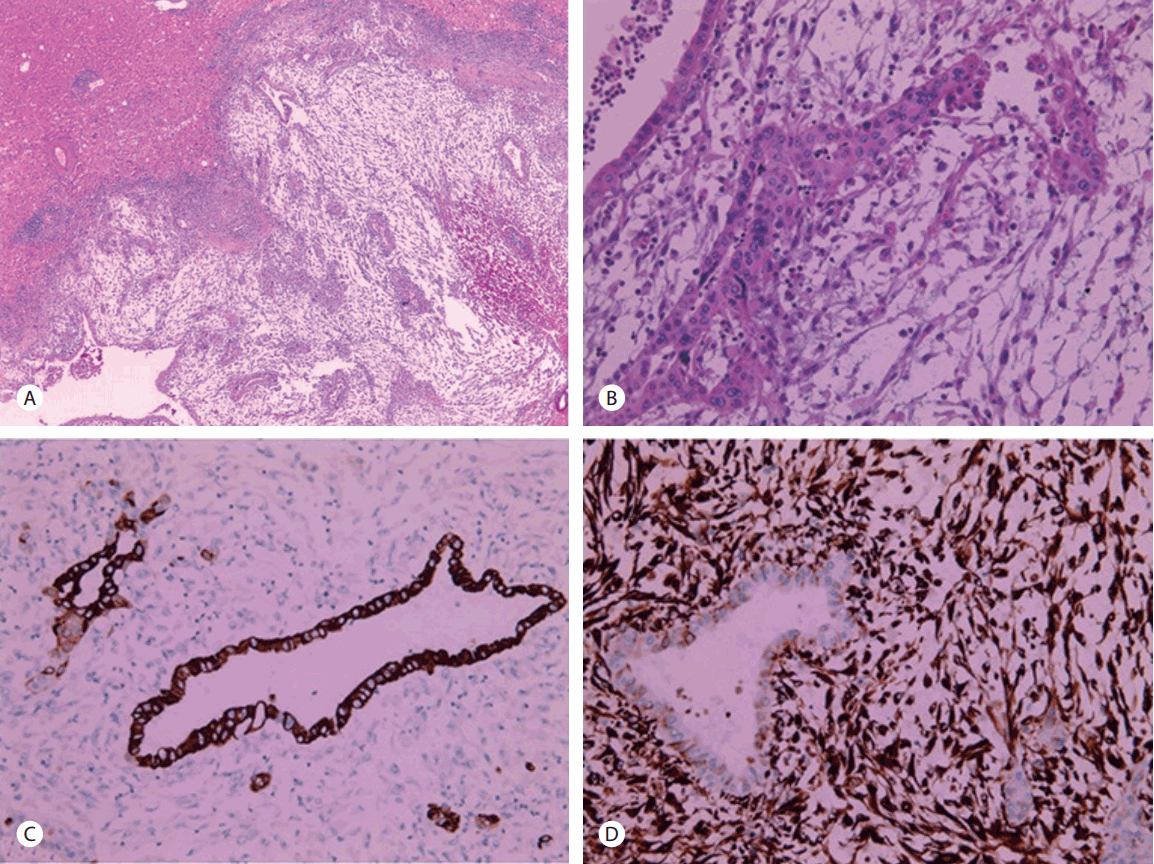
Table 1.
Summary of cases of intrahepatic sarcomatoid cholangiocarcinoma in the literature
|
Reference |
Age/Sex |
Sarcomatoid component |
IHC |
Initial Treatment |
Recurrence after surgery/second-line treatment |
Outcome |
|
Malhotra, et al.
|
60/F |
Pleomorphic and spindle cells |
CK19 (+)/Vimentin (+) |
Surgery |
(+)/Gemcitabine plus Cisplatin CTX |
Alive beyond 29 months after diagnosis |
|
Kim, et al.
|
68/F |
Spindle cells with rhabdoid transformation |
CK7 (+)/Vimentin (+) |
CTX |
NA |
Died within 1 month after diagnosis |
|
Jung, et al. |
59/M |
Undifferentiated spindle cells |
PAN-CK (+)/ Vimentin (+) |
Surgery with adjuvant CTX |
(+)/Gemcitabine plus Cisplatin CTX |
Alive beyond 8 months after diagnosis |
|
Hong, et al. |
69/F |
Pleomorphic and spindle cells |
CK19 (+)/Vimentin (+) |
None |
NA |
Lost to follow-up |
|
Inoue, et al.
|
61/M |
Undifferentiated spindle cells |
CK7 (+)/Vimentin (+) |
Surgery |
(+)/(-) |
Died within 2 months after diagnosis |
|
Sato, et al.
|
87/M |
Round cell variant |
CK19 (+)/Vimentin (+) |
None |
NA |
Died within 3month after diagnosis |
|
|















