서 론
신경절세포 부신경절종(gangliocytic paraganglioma)은 흔하지 않은 소화기계 종양으로 대부분 십이지장에서 발견되며, 조직학적으로 부신경절종과 유사한 상피양세포, 방추형 세포 및 신경절세포를 확인하여 진단할 수 있다[1].
이소성 췌장은 췌장 고유 조직과 해부학적으로 떨어져 다른 부위에 위치하는 췌장 조직으로[2], 식도로부터 항문까지 전 위장관에서 발생할 수 있으며[3] 그 위치에 따라 다양한 증상이 발현될 수 있으나, 주로 증상이 없이 우연히 발견된다[2,3].
국내에서는 십이지장, 특히 바터팽대부에 발생한 신경절 세포 부신경절종과[1,4] 십이지장의 이소성 췌장의 증례[5]가 각각 드물게 보고되었으나 아직까지 신경절세포 부신경절종과 이소성 췌장이 동시 발현된 보고는 없었다. 국외에서는 Lau 등[6]이 십이지장에 발생한 신경절세포 부신경절종이 이소성 췌장에서 유래하였다고 보고하였다. 저자들은 상복부 불편감으로 발견된 바터팽대부의 점막하 종양에 대해 진단 및 치료를 위해 내시경적 절제술을 시행 후 신경절세포 부신경절종과 이소성 췌장이 동시 발견된 증례를 경험하여 문헌 고찰과 함께 보고하는 바이다.
증 례
39세 여자가 한달 동안 지속된 상복부 불편감을 주소로 내원하였다. 과거력 및 가족력상 특이 소견은 없었으며 입원하여 시행한 초기 활력 징후상 혈압은 120/68 mmHg, 심박수 68회/분, 호흡수 20회/분, 체온 36.4°C였다. 이학적 검진상 우상복부 압통을 호소하였으며 흉부 청진에서 호흡음, 심음은 모두 정상이었다.
일반 혈액검사에서 백혈구 6,000/mm3, 혈색소 12.9 g/dL, 혈소판 232,000/mm3였고 혈청 생화학검사에서 총 단백 6.9 g/dL, 알부민 4.2 g/dL, 총 빌리루빈 0.27 mg/dL, 아스파라진산아미노전이효소 16 IU/L, 알라닌아미노전이효소 18 IU/L, 알칼리성인산분해효소 65 IU/L, 감마글루타밀전이효소 29 IU/L, 아밀라아제 46 IU/L, 리파아제 29 IU/L, 혈액요소질소 9.8 mg/dL, 크레아티닌 0.6 mg/dL로 정상이었다. 혈청 전해질검사에서 나트륨 140 mEq/L, 칼륨 4.2 mEq/L, 염소 104 mEq/L, 인 3.8 mg/dL, 칼슘 9.2 mg/dL, 마그네슘 1.9 mg/dL로 정상 소견을 보였다.
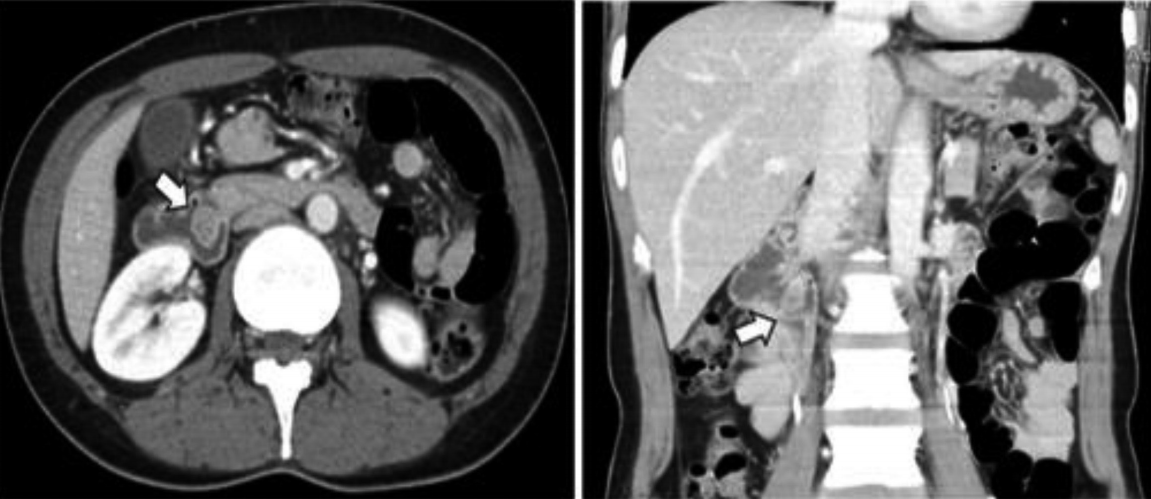
복부 전산화단층촬영에서 바터팽대부 근처에 위치한 약 1.4 cm 정도의 비교적 윤곽이 분명한 조영증강이 잘 되는 계란형의 종괴가 관찰되었으며(Fig. 1) 병변 주변의 이상 림프절비대나 원격장기 전이소견은 관찰되지 않았다.
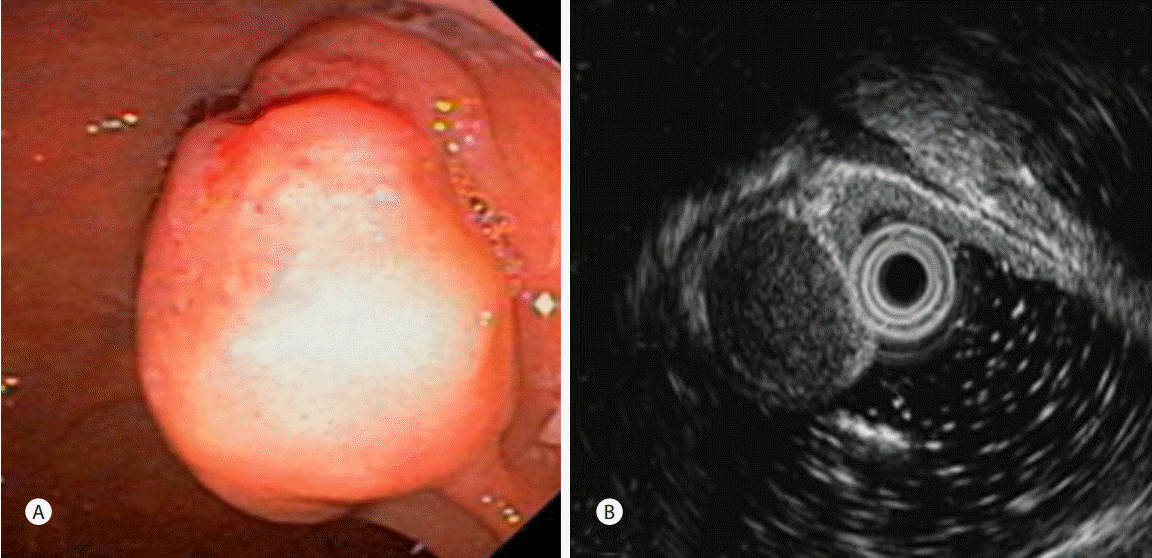
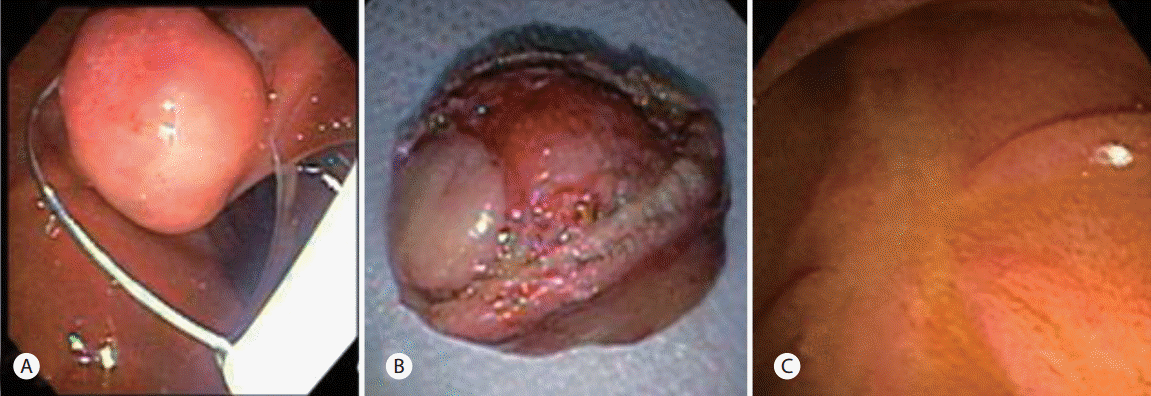
상부위장관 내시경검사에서 바터팽대부에 개구부를 포함하고 돌출된 상피하 종양이 관찰되었으며, 내시경초음파검사에서 점막하층에 약 14 mm 정도의 비교적 균질한 저에코의 점막하 종양으로 확인되었다(Fig. 2). 주변의 림프절비대 소견은 없었고 담관 및 췌관의 침범이 없었으며 병변은 십이지장 벽의 고유근층은 침범하지 않아 내시경적 절제가 가능할 것으로 판단하였다. 진단 및 치료를 위해서 측시경을 이용하여 내시경적 절제술을 시행하였다(Fig. 3A). 병변은 충분히 십이지장 내강 내로 돌출되어 있었고 점막하층 병변으로 에피네프린 주입시 종양의 범위를 파악하기 어렵기 때문에 에피네프린 주입 없이 바로 올가미를 이용하여 절제를 시행하였다. 절제시 유두 개구부가 절제 부위에 포함되어 췌장염을 예방하기 위해 내시경적역행성담췌관조영술을 시행하고 췌관에 플라스틱스텐트를 삽입하였다.
절제된 조직의 육안적 소견을 살펴보았을 때 원형으로 회색조를 띄고 다소 단단한 병변과 그 주변으로 약간 부드러운 분홍빛의 병변이 관찰되었다(Fig. 3B). 육안적 병리 소견상 종양의 크기는 2 × 1.5 × 1.2 cm였으며 절제된 검체의 병리 결과에서 병변은 십이지장 제2부 점막하층에 위치하였고 절제부의 경계부 침범 및 혈관 침범은 관찰되지 않았다. 현미경 소견을 보면 유사분열은 관찰되지 않았으며 헤마톡실린 및 에오신(hematoxylin and eosin, H & E) 염색상 두 개의 각기 다른 병변 소견이 관찰되었는데, 한 곳은 주로 췌장 샘꽈리 조직이 엽상 증식을 하는 췌장 조직을 관찰할 수 있어 이소성 췌장으로 진단되었다(Fig. 4A). 그리고 주된 종양 조직은 단조로운 상피세포성 군집이 둥글거나 죽상 모양의 배열을 보이고 있으며 그 주변으로 풍부한 혈관 조직을 관찰할 수 있어 보편적인 부신경절종의 소견으로 판단하였다(Fig. 4B). 그리고 부분적으로는 신경절 모양이나 방추형 핵을 가진 세포들이 통상적인 상피성 종양 조직과 섞여 있는 양상 또한 관찰할 수 있어 이는 신경절세포 부신경절종에 부합하는 소견이었다(Fig. 4C, D). 최종적으로 면역조직학검사에서 chromogranin, CD56, synaptophysin 그리고 S-100 염색 양성 소견을 보여 신경절세포 부신경절종으로 진단되었다(Fig. 5). 이 두 병변은 서로 독립적으로 존재하였으며 이행부위(transitional zone)는 없었다(Fig. 4A).
환자는 내시경적 절제술 후 양호한 경과를 보여 퇴원하였으며 이후 약 2년간의 지속된 추적관찰 상에 종양의 재발이나 전이 소견은 관찰되지 않았다(Fig. 3C).
고 찰
신경절세포 부신경절종은 드문 점막하 종양으로 부신경절종과 유사한 상피양세포, 방추형세포 및 신경절세포의 구성으로 이루어진 신경내분비 종양이다. 주로 십이지장의 제2부에서 발생하나 위 및 근위부 공장 등에서도 발생할 수 있다[7]. 남성이 여성보다 더 많으며(1.5-6:1)[4] 발생 연령은 23세에서 83세까지 다양하나 주로 50대에 발생빈도가 높다. 대부분 무증상인 경우가 많으나 발생 위치에 따라 복통, 위장관 출혈, 폐쇄 등이 나타날 수 있다[7,8]. 형태학적 소견으로 크기는 0.5 cm에서 10 cm까지 다양하며 대부분 유경성 종괴의 양상을 보이며 점막하 단일 병변으로 발견된다[7].
신경절세포 부신경절종은 조직학적으로 부신경절종과 유사한 상피양세포, 방추형세포 및 신경절세포의 세가지 세포로 구성되어 있으며, 그 성분 간의 구성 비율은 다양하다. H & E 염색으로 위의 세가지 세포 성분을 확인하여 진단할 수 있으며[8] 면역조직화학 검사를 통해 각 세포의 성상을 구분할 수 있다. 일반적으로 면역조직화학 검사에서 방추형 세포는 S-100, neurofilament protein 등에 양성 반응을 보이고 일부에서는 CD56에 양성을 보인다. 신경절세포는 neuron-specific enolase, synaptophysin, somatostatin, CD56에 양성이며, 상피양세포는 chromogranin, serotonin, somatostatin, CD56 등에 양성 반응을 보이고 일부에서 neuron-specific enolase, cytokeratin 등에 양성 반응을 보인다[9,10]. 본 증례의 경우 종양 조직이 세 가지 세포로 구성되어 있고 상기한 신경내분비 표지에 양성 소견을 보이며 신경절세포 및 방추형 세포는 매우 국소적으로 관찰할 수 있는 증례이다.
이소성 췌장은 췌장 고유 조직과 해부학적으로 떨어져 다른 부위에 위치하는 췌장 조직으로[2] 식도로부터 항문까지 전 위장관에서 발생할 수 있으며 그 위치에 따라 다양한 증상이 발현될 수 있으나, 증상이 없이 우연히 발견되는 경우가 대부분이다[3]. 이소성 췌장은 정상 췌장에서 나타날 수 있는 모든 병적 변화가 발생하며 급성 및 만성 췌장염, 낭종, 농양, 출혈 및 괴사, 양성 및 악성 종양 등이 나타날 수 있다. 이소성 췌장에서의 악성 변화는 고유 췌장 조직보다 더 많은 빈도로 발생한다는 보고가 있으나[2] 임상적으로 이소성 췌장의 악성 변화는 흔하지 않으며 약 0.7%에서 악성 변화를 관찰하였다는 보고가 있었다[11]. 한편 바터팽대부에 발생되는 이소성 췌장은 매우 드물며 간혹 담관 폐쇄에 의한 황달 또는 복통을 일으킬 수 있다[12].
십이지장의 신경절세포 부신경절종의 조직학적 발생 기원은 아직 확실히 밝혀지지 않았으나 Perrone 등[13]은 췌장의 복측 원기에서 유래한 상피세포의 과오종성 증식이라고 제안하였고 이소성 췌장 조직에서 발생한 분리종 혹은 과오종이라는 주장과[7] 배아 복강 신경절에서 발생한다는 가설[14], 창자샘의 기저부에 있는 다능성 줄기세포에서 기원한다는 의견 등이 있다[15]. 이 중 Burke와 Helwig [7]은 51명의 신경절세포 부신경절종 환자를 대상으로 연구를 시행하였는데, 51명의 환자 중 대다수에서 췌장형 관 조직이 발견되었으며 췌장 폴리펩티드 염색이 양성으로 관찰되었다. 이로 인해 Burke와 Helwig [7]은 신경절세포 부신경절종이 이소성 췌장 조직에서 발생한 분리종이라 주장하였다. 본 증례에서도 절제된 조직에서 췌장 조직과 신경절세포 부신경절종이 동시에 관찰되어 Burke와 Helwig [7]의 주장과 일치하나 명확한 이행부위가 관찰되지 않아 이소성 췌장과 신경절세포 부신경절종의 연관성에 대해서는 추후 더 많은 연구가 필요하겠다.
신경절세포 부신경절종은 대부분 임상적으로 양성 종양의 경과를 보이며 재발 및 국소 림프절전이는 드물어 수술 전에 정확한 진단을 하는 것이 중요하나, 실제로는 수술 전 정확한 조직 진단을 하기가 어려워 췌십이지장절제술과 같은 과도하게 광범위한 수술을 시행하는 경우가 많다. 따라서 점막하 종양인 경우 내시경 초음파로 종양의 존재 층이 점막하층에 있다는 것을 진단하고 국소 림프절전이 및 주변 조직으로의 침윤이 없다면 종양을 내시경적으로 국소적인 절제를 시행할 수 있으며 이로 인해 불필요한 수술 및 수술로 인한 합병증을 피할 수 있을 것이다.
본 증례에서는 상부위장관 내시경 및 내시경초음파로 확인된 바터팽대부 점막하 종양에 대해 진단 및 치료를 위해 내시경적 절제술을 성공적으로 시행하였고 절제된 종양 내에 신경절세포 부신경절종과 이소성 췌장이 공존하는 것으로 진단되었다. 이는 아직 국내에서 보고된 바가 없어 상기 두 병변이 공존하는 것의 발견에 의의가 있으며 그 연관성에 대해서는 추후 더 많은 연구가 필요할 것으로 생각된다.