증상 없는 아밀라아제, 리파아제 증가에 대한 평가
요약
건강검진이나 혈액검사의 일부로 혈청 췌장효소 수치의 상승이 발견되는 경우가 증가하고 있으나, 증상이 뚜렷하지 않은 아밀라아제와 리파아제 수치 상승의 임상적 중요성은 불분명하다. 췌장효소가 상승한 환자를 진료할 때, 급성 췌장염, 간기능 장애, 신장기능 부전과 같은 흔한 원인은 철저한 병력청취, 신체검진 및 기본적인 혈액검사로 우선 배제해야 한다. 복부 초음파 또는 전산화단층촬영, 지질 프로필, 종양표지자, 이소효소 및 amylase-to-creatinine clearance ratio 계산 또는 polyethylene glycol 침전검사 등 다양한 테스트를 통하여 다양한 원인에 대한 가능성을 타진해보고 배제한다. 췌장효소가 명백한 원인 없이 반복적인 검사에서 지속적으로 상승한 경우, 만성 비병인성 혈중 췌장효소증가증(CNPH)으로 진단하게 된다. CNPH 환자에 동반된 양성 질환의 임상적 의미에 대한 해석은 연구자들에 따라 다양한데, 동반소견의 대부분은 양성의 질병 경과를 나타낸다. 자기공명담췌관촬영술(MRCP)은 CNPH 환자에게 매우 유용하고 중요하며, 세크레틴 자극 자기공명담췌관촬영술(MRCP-S)은 아직까지 국내에는 허가되지 않아 임상적 적용은 어렵다. 의사의 선호도에 따라 내시경 초음파를 통해 평가할 수 있지만 침습적인 측면이 있어 주기적인 추적관찰에는 적합하지 않다. CNPH와 연관된 양성 췌장질환에 대한 적극적인 치료 또는 정기적 추적관찰의 필요성을 고려한 후, 발견된 소견에 대한 개별적인 접근이 필요하다. CNPH 환자에서 진단을 위해 시행해야 하는 검사의 범위 그리고 동반된 양성 소견의 임상적 중요성과 추적관찰의 방식 및 종료시점에 대해서는 현재까지의 연구가 제한적이고 전문가들의 의견이 일치하지 않기에 향후 다양한 장기 데이터가 보고될 때까지는 결론을 내리기 어렵다.
Keywords: 췌장, 아밀라아제, 리파아제
Abstract
There are increasing number of cases of serum amylase and lipase levels being examined as part of health screening, but the clinical significance of these amylase and lipase levels is unclear. When the clinicians encounter patients with elevated pancreatic enzymes, the most common causes such as acute pancreatitis, hepatic or renal dysfunction should be ruled out first by thorough history taking, physical examination, and laboratory tests. Further tests including abdominal ultrasonography or computed tomography, lipid profile, tumor marker, isoenzyme, and calculation of amylase-to-creatinine clearance ratio or polyethylene glycol precipitation test should be performed to exclude other causes. If the pancreatic enzymes are continuously elevated through repeated tests without any apparent etiology, the diagnosis is made with chronic non-pathological pancreatic hyperenzymemia (CNPH). Magnetic resonance cholangiopancreatography is very useful and important modality for the patients with CNPH but the clinical significance of magnetic resonance cholangiopancreatography with secretin stimulation is still unclear. They can be evaluated through endoscopic ultrasonography with preference but it is less suitable for follow-up. Individualized approaches should be made after considering the need for active treatment or periodic follow-up for the benign pancreatic diseases associated with CNPH. It is difficult to conclude until more long-term data are reported because there are only limited number of researches and consensus on the range of tests to be performed for diagnosis, clinical significance of benign findings and end of follow-up in patients with CNPH.
Keywords: Pancreas, Amylase, Lipase
서 론
췌장은 95%의 외분비조직과 5% 미만의 내분비조직으로 이루어져 있으며 외분비조직은 소화기능을 담당하는 효소들을 분비한다. 혈청 아밀라아제 및 리파아제는 상이한 조직으로부터의 생산 및 제거의 균형을 반영하지만, 수많은 분자, 세포 및 시스템 기작에 의해 영향을 받을 수도 있다[ 1]. 아밀라아제와 리파아제는 췌장염에서 주로 검사를 하는 효소로 췌장염을 진단하기 위해서는 이러한 상승된 효소와 임상양상이 부합해야 한다. 최근 증상은 없으나 건강검진 혹은 혈액검사의 일환으로 혈청 아밀라아제, 리파아제 수치를 검사하는 경우가 늘어나고 있으며 이들이 어떤 임상적인 의의를 가지는지는 명확히 정립된 바가 없는 상태이다. 이번 종설에서는 이러한 아밀라아제와 리파아제의 상승이 어떤 의의를 가지는지, 특히 호소하는 증상이 없을 경우 임상에서 어떻게 대처해야하는 것이 좋을지 살펴보고자 한다.
본 론
아밀라아제 및 리파아제의 생성과 대사
아밀라아제는 주로 췌장과 침샘에서 분비하는 소화효소로써 알파-1,4-글리코시드 결합을 가수분해하여 전분을 작은 탄수화물 그룹으로 나누고 최종적으로 이당류나 올리고당류로 만들어준다. 아밀라아제는 주로 췌장과 침샘에서 대부분이 분비되며 그 외 나팔관, 고환, 폐, 갑상선, 편도, 유선조직, 땀샘, 눈물샘 등에서도 생성된다. 이러한 아밀라아제는 혈중에서도 검출이 되는데, 건강한 성인에서 혈중 아밀라아제는 췌장에서 분비되는 아밀라아제(P-type)가 40-45%, 침샘에서 분비되는 아밀라아제(S-type)가 55-60% 정도를 차지한다[ 2]. 리파아제 역시 주로 췌장에서 분비하는 소화효소로서 지방을 가수분해하여 흡수 가능한 형태로 분해하는 역할을 한다. 췌장에서 분비된 리파아제는 99%가 십이지장으로 분비되고 나머지 1%가 림프와 모세혈관으로 분비된다. 췌장 이외에도 위, 십이지장, 소장, 대장, 심장, 간 및 혀에서도 리파아제가 생성된다[ 3, 4]. 혈중 아밀라아제와 리파아제는 그 기원과는 무관하게 25% 정도는 신장에서 배설되는데 아밀라아제는 세뇨관에서 일부 흡수되고 리파아제는 거의 대부분 재흡수된다. 아밀라아제는 세망내피계(reticulo-endothelial system)에 의해 제거되는 것으로 알려져 있어 간이 매우 중요한 역할을 하는 것으로 알려져 있다[ 1]. 이러한 사실은 몇몇 연구에 의해서 확인되었는데[ 5], 만성 신부전 환자들 중 사구체여과압이 50 mL/min 이하로 감소된 환자들에서 정상인 환자들에 비해 아밀라아제 농도가 높게 측정되며, 간괴사 및 간경변 환자에서도 아밀라아제가 높게 측정된다[ 6].
혈청 아밀라아제와 리파아제 상승의 가능한 원인들
1. 일반적인 접근
임상에서 많이 검사하는 대표적인 췌장효소인 혈청 아밀라아제와 리파아제는 급성 췌장염의 진단에 매우 중요하다. 이들 효소 수치의 상승이 췌장과 연관이 없을 수도 있고, 췌장염이 있지만 효소 수치는 정상인 경우도 있기 때문에 이 검사 결과를 환자에 맞게 적절하게 해석해야 한다. 췌장효소 상승이 발견된 환자에서 무엇보다 가장 중요한 것은 병력청취 및 신체검진이다. 급성 췌장염에 합당한 병력 및 검진소견을 보이는 경우에는 췌장염을 유발할 수 있는 다양한 원인에 대한 감별이 필요하다. 음주력이나 약물복용력, 담석 여부 확인 등 흔한 원인에서부터 자가면역췌장염, 췌장 악성 질환 등에 드문 원인도 최대한 염두에 두고 접근해야 한다. 급성 췌장염을 진단하기 위해서는 췌장효소가 정상 상한선의 3배 이상 상승한것을 진단기준으로 많이 이용하고, 이때 아밀라아제의 민감도는 85%, 특이도는 91%인 반면[ 7], 리파아제는 아밀라아제보다 특이도가 더 높아서 약 98%에 달한다[ 8]. 또한 혈청 아밀라아제가 리파아제보다 더 빨리 감소하기 때문에 급성 췌장염의 진단에 있어서 리파아제가 더 유용하다는 의견이 우세하다. 하지만 혈청 아밀라아제와 리파아제 수치가 급성 췌장염의 중증도와는 관련이 없는 것으로 알려져 있고[ 9], 혈청 아밀라아제와 리파아제 수치가 급성 췌장염 상황에서도 정상일 수 있다는 점도 염두에 두어야 한다[ 10]. 기타 아밀라아제 이소효소, phospholipase A2, elastase1, anionic trypsinogen 등도 연구되었으나 여전히 임상적으로 사용되고 있지는 못하고 있다[ 11]. 췌장효소가 상승해 있는 경우 가장 흔하게 상기와 같이 췌장염을 의심할 수 있으나 췌장염이 의심되지 않는 경우, 면밀한 병력청취와 신체검진, 동반된 혈액검사 등을 통해서 다른 췌장질환을 비롯하여 효소의 상승을 설명이 가능한 췌장 외의 다른 원인이 동반되어 있는지 꼼꼼히 살피는 것이 중요하다. 췌장효소 수치의 상승이 확인된 환자에 대해서 아직까지 잘 정립된 가이드라인은 없지만, 병력 등 임상양상에 대해 충분히 고려한 후 추가 검사를 진행하는 것을 원칙으로 해야 한다. 즉, 췌장염 이외에 전신질환, 약물, 췌장의 구조적 이상, 만성 비병인성 혈중 췌장효소증가증(chronic non-pathological pancreatic hyperenzymemia, CNPH) 등에 대한 고려가 필요하며, 진단이 확실하지 않은 경우 복부 초음파, 전산화단층촬영(computed tomography, CT)이나 자기공명담췌관촬영술(magnetic resonance cholangiopancreatograpy, MRCP)이 진단에 도움이 될 수 있다. 현재까지의 연구 결과를 바탕으로 하였을 때, Fig. 1과 같은 진단 알고리즘을 생각해볼 수 있다. 췌장질환과 무관한 췌장효소 수치의 상승은 췌장 이외의 장기에서의 문제, 신장기능저하 또는 macroamylasemia로 인하여 신장 배설이 감소하는 문제로 나누어 접근해야 하는 것이 일반적이다. 기본적으로 췌장 이외의 원인으로 인종, 배설 장애를 유발할 수 있는 간/신기능 장애, 사용약물 등에 대하여 확실히 확인하는 것이 필요하다[ 1]. 앞서 살펴본 효소의 제거기전에 비추어보면, 신장기능이 감소하거나 간 손상이 있는 경우에 췌장효소가 상승할 수 있으리라 생각된다. 아밀라아제가 면역글로불린이나 다당류와 같은 고분자물질에 붙어서 macroamylase를 만드는 경우 신장배설이 어렵게 되어 혈중 아밀라아제 수치가 만성적인 상승소견을 보일 수 있으며, 혈중 아밀라아제 농도는 일중 변화를 보인다[ 12]. 이러한 macroamylasemia를 유발할 수 있는 질환은 셀리악병(celiac disease), 인간면역결핍바이러스(human immunodeficiency virus) 감염, 림프종, 궤양성 대장염, 류마티스관절염, 단클론성 감마글로불린 장애(monoclonal gammopathy) 등이 있다고 알려져 있으며[ 13, 14], 셀리악병 환자가 글루텐 프리 식이(gluten-free diet)를 하는 경우 macroamylasemia도 같이 호전되는 것으로 알려져 있다. 이러한 macroamylasemia를 진단하기 위해서는 혈청 아밀라아제에 대한 면역학적 분석을 통해 분자량 측정을 하거나, 아밀라아제와 크레아티닌의 제거율 비교(amylase-to-creatinine clearance ratio; [urine amylase/serum amylase] × [serum creatinine/urine creatinine] × 100, reference 1-4%)를 통해 감소되어 있는 경우 진단이 가능하다[ 15].
2. 고아밀라아제혈증과 고리파아제혈증
혈청 아밀라아제와 리파아제의 농도가 오를 수 있는 상황에 대해서 Table 1에 정리하였다. 고아밀라아제혈증이 있을 경우 췌장 혹은 췌장 주변의 원인, 그리고 비췌장 원인으로 구분해 볼 수 있는데, 췌장 혹은 췌장 주변의 원인은 가성낭종, 췌장복수, 악성 종양, CNPH가 있으며, 비췌장 원인으로는 인종, 침샘문제, macroamylasemia, 종양에 의한 것이 있다. 만성 고아밀라아제혈증의 원인으로 췌장염, 가성낭종, 또는 췌장복수가 제시되기도 하지만, 많은 환자에서는 이와 연관된 췌장질환을 밝히지 못한다[ 16]. 비췌장성 고아밀라아제혈증의 대표적인 것들로 salivary hyperamylasemia, 침샘 장애, 신경성 식욕부진이나 폭식증 같은 섭식 장애, 종양에 의한 것이 있다. 매우 다양한 종양에서 고아밀라아제혈증이 발생할 수 있는데, 종양에서 효소의 과생성이 발생하기도 하고 염증반응으로 인해 조직에서 효소가 과분비되기도 한다. 난소종양, 폐암, 다발성 골수종, 갈색세포종에서는 거의 대부분 침샘 기원의 아밀라아제(S-type)로 확인된다[ 16]. 췌장염이 아닐 경우 리파아제가 상승하는 경우는 여러 가지 상황이 있으며 대표적으로는 급성 신손상이 있으나 그 원인과 리파아제는 특별한 상관관계가 없다. 셀리악병과 염증성 장질환은 리파아제 상승과 연관이 있으나 일반적으로 정상 상한치의 3배 이상 상승시키지는 않는다. 이외에도 증상이 없는 일부 일부 C형 간염 바이러스(hepatitis C virus) 보유자와 인간면역결핍바이러스 보유자에서 리파아제 상승이 확인된다. 간암이나 대장 혹은 소장암의 간전이, 위암의 전이시 혈중 리파아제는 정상의 상한치보다 3배 이상 상승할 수 있다. 내시경적 역행성 담췌관조영술(endoscopic retrograde cholangiopancreatography, ERCP) 후에도 췌장염 증거 없이 혈청 리파아제 상승이 관찰되기도 한다. 다발성 외상 환자에서 두부손상이 없는 경우 영상이나 수술장 소견에서 췌장염의 증거가 없더라도 리파아제 수치가 상승하기도 한다[ 17]. 한 연구에 따르면 무증상의 제2형 당뇨병을 진단받은 일부 환자에서 혈청 리파아제가 정상 상한치의 3배 이상 상승할 수 있다고 한다[ 18]. 그리고 사르코이드증(sarcoidosis)이 혈청 리파아제를 정상 상한치의 3배 이상 상승시키는 원인이 될 수 있다는 보고가 있다[ 19]. 췌장효소 상승과 연관된 약물도 많이 알려져 있는데, 췌장염을 동반할 수도 안 할 수도 있으며 췌장효소를 상승시키는 기전이 명확히 알려져 있지 않은 경우가 많다. Paracetamol, steroid, azathioprine, ephedrine, ritodrine, roxithromycin, cyclosporine, clozapine, pentamidine, didanosine 등이 알려져 있다.
만성 비병인성 혈중췌장효소증가증(CNPH; Gullo’s syndrome)
1. CNPH의 의미
췌장질환의 증거가 없는 혈중 췌장효소의 상승은 1970년대 Warshaw와 Lee [ 20]가 보고한 바 있으며 그들은 췌장이 잘못되었다는 가정 하에 과도한 치료를 할 수 있음을 지적하였다. 1996년 Gullo 등[ 21- 24]은 무증상이며 6개월 이상의 만성 췌장효소의 상승소견을 보이는 경우를 보고하며 CNPH라는 용어로 정의하였으며, 후에 이는 “benign pancreatic hyperenzymemia” 또는 “Gullo 증후군” 등으로 불리고 있다. Gullo 증후군은 산발성(sporadical) 혹은 가족성(familial) 형태로 나타나며 아밀라아제 및 리파아제의 수치의 변동이 하루 동안에도 발생하고 추적관찰 중 정상치까지 내려왔다가 정상치의 10배 이상으로 높아지는 등 변동이 심하게 관찰되는 환자에서 특별한 원인이 없는 경우를 새로운 질병군으로 정의한 것이며, 대부분은 췌장효소가 정상치의 2-4배 정도 상승한 것으로 측정된다. 아마도 유전적인 문제가 있다고 생각되지만 아직 정확한 원인은 규명되지 못하였다. CFTR, SPINK1, PRSS1 등의 gene mutation과는 관계가 없고, 확진을 위해서는 최소 1-2년간의 추적관찰이 필요하다[ 21]. Gullo 등[ 24]은 이러한 췌장효소의 상승을 보이는 환자들이 특별한 질병이 없을 가능성이 높음에도 불구하고 많은 검사를 시행받게 되고 의료비 지출을 과도하게 하는 점을 지적하며 환자를 안심시킬 필요가 있다고 주장하였다. 하지만 임상에서 이러한 상황의 환자가 외래에 방문하였을 때, Gullo 증후군으로 결론을 내리고 안심시키는 것은 쉬운 일이 아니다. 그 이유는 모든 췌장 관련 질병이 배제되어야 하고, 진단 후 다른 검사들이 전혀 필요하지 않은 것이 확실하다는 전제가 있어야 하기 때문이다.
2. CNPH의 평가
최근까지 CNPH 환자들을 대상으로 한 후속 연구들이 꾸준히 이루어지고 있으며, 췌장의 구조 및 기능의 문제에 대한 검사를 시행하는 방법의 발전으로 췌장의 선천적 구조이상, 췌관이상소견, 조기 만성 췌장염(early chronic pancreatitis) 의심소견, delayed main pancreatic duct emptying, 췌장의 낭성종양(pancreatic cytic lesions, PCLs), 췌장의 내분비종양, 췌관확장, 분할췌 등이 이와 같은 췌장의 구조 및 기능이상이 CNPH 환자들에게서 보고되고 있으며 그 결과를 Table 2에 정리하였다. 복부 초음파는 간편하고 실시간으로 정보를 얻을 수 있으며 인체에 해가 없어 첫 검사로 시행할 수 있으나 민감도가 낮고 검사자에 대한 의존도가 높으며 일부 환자에서 검사의 질이 떨어진다. 현재까지 췌장염의 진단에 표준검사인 CT가 췌장의 검사에 매우 유용하지만, 췌장의 미세한 변화는 확인이 힘들고 방사선노출 및 조영제로 인한 부작용이 발생할 수 있다. ERCP는 췌관의 변화를 가장 잘 관찰할 수 있고, 만성 췌장염의 진단의 표준검사이지만 합병증이 3-7% 정도 발생하기에 단순 진단목적보다는 치료적 목적으로 시행한다. 최근에는 내시경초음파(endoscopic ultrasonography, EUS), MRCP, 세크레틴 자극 자기공명췌담관조영술(MRCP with secretin stimulation, MRCP-S) 등의 검사법들을 병합하여 가능한 췌장의 이상소견을 모두 발견하기 위한 시도들이 이루어지고 있으나 국내에서는 아직까지 MRCP-S는 허가되지 않아 사용되고 있는 기관이 거의 없다. MRCP의 경우 췌장의 구조이상을 진단하는데 유용하며, MRCP-S의 경우 특히 측분지 췌관(side branch pancreatic duct)의 이상소견 및 delayed main pancreatic duct emptying을 진단하는 데에 유용하다[ 25- 28]. EUS의 경우도 췌관 및 췌장의 실질에 있는 다양한 병변에 대하여 민감도가 매우 높은 검사이며 특히 만성 췌장염의 진단에 다른 검사들에 비하여 유용하다[ 28, 29].
3. CNPH의 일반적인 접근
CNPH는 대부분 양성 소견에 동반되는 것으로 보여지며, 현재까지 발표된 CNPH 환자에서 진단을 위한 검사를 시행한 결과를 종합해보면( Table 2), 8.2-68.7%에서 췌장의 형태학적, 기능적 이상소견이 보고된 바 있다. 그중 2 개의 연구에서는 췌장 선암이 보고된 바 있는데[ 27, 30], Pezzilli 등[ 30]이 보고한 연구에서는 4% (75명 중 3명)에서 췌장 선암이 진단되었으며, 이들 중 두 명은 각각 진단 후 3개월과 14개월에 사망하였다. 다만 이 연구 대상자들의 최종진단에서 자가면역성 췌장염과 크론병 환자들이 포함되어있어 환자 선정과정에서 제한점이 있는 것으로 생각된다[ 30]. 췌장 선암을 보고한 또 다른 연구에서는 증상을 호소하는 환자들이 많이 포함된 연구로 진정한 의미의 CNPH 환자에서 발생한 결과로 받아들이기는 어렵다[ 27]. 따라서 임상적으로 병력청취, 신체검진, 기본 검사 등에서 기질적 질환의 증거가 전혀 없는 경우에는 대부분 양성 질환에 동반된 췌장효소 상승소견으로 보고 접근을 할 수 있다. CNPH로 환자를 진단하기 위해서는 오랜 관찰 기간과 반복되는 혈액검사와 다양한 영상검사들이 시행되어야 하므로 환자의 경제적 부담이 가중되고 삶의 질이 저하된다. 그렇다면 어떤 검사를 언제까지 시행하는 것이 타당할 것인가? 사실 이에 대한 결론을 내기 위해서는 현재까지 시행된 연구가 매우 제한적이며 대부분이 후향적 관찰연구이다. 최근의 MRCP, MRCP-S, EUS를 이용한 연구 결과들이 보고되었는데, 조기 만성 췌장염에 대한 MRCP의 민감도와 특이도는 각각 92%, 75% 정도이며[ 31, 32], MRCP를 통한 췌장의 낭성병변의 발견율은 2.4-19.6% 정도로 보고되어 기존에 보고된 부검자료와 큰 차이를 보이지 않았다[ 32- 34]. 일부 연구자들은 MRCP-S를 이용하여 조기 만성 췌장염의 진단율을 높일 수 있기에 MRCP-S의 필요성을 역설하고 있으며[ 35, 36], MRCP에 비해 MRCP-S를 이용하면 췌관의 확장소견을 더욱 명확히 확인할 수 있음이 보고된 바 있다[ 25, 27]. 하지만 MRCP-S를 통해 추가로 발견되는 소견들 역시 양성소견이라는 점을 고려해볼 때, 그 임상적 의의는 여전히 제한적이며 MRCP-S를 시행 가능한 기관도 일부 기관에 국한된다는 점에 있다는 점 역시 제한점으로 작용한다. 또한, 일부 연구자는 EUS를 이용하면 췌관내유두상점액종양(intraductal papillary mucin-producing neoplasm, IPMN)의 진단이나 조기 만성 췌장염의 진단에 용이하기에 MRCP-S와 EUS 모두 시행하여 췌장의 이상을 확인해야 한다고 주장한다[ 37]. 그러나 EUS는 검사가 고비용이면서 침습적이고, 검사자에 대한 의존도가 높아 Rosemont criteria 등을 이용하더라도 조기 만성 췌장염의 진단에 있어서 정확도가 좋지 않다는 한계점이 있어 MRCP-S에 비해 우수성 및 적합성이 증명되었다고 보기 어렵다[ 29]. 종합해보면, CNPH 환자를 진료함에 있어서 복부 초음파나 CT만을 시행하기보다는 추가적으로 MRCP를 이용한 평가가 필요할 것으로 보이며, MRCP-S의 경우 임상적 의의가 뚜렷하지 않으며, 앞서 언급한 것처럼 국내에서는 허가가 되지 않아 활용이 어려운 실정이다. 검사자의 숙련도나 센터의 상황 및 환자의 상황에 맞추어 MRCP 대신 EUS를 통한 평가해볼 수 있으나 반복적인 추적관찰을 위한 검사로서 EUS는 무리가 따른다. 더불어 CNPH가 진단된 환자에서 재검사 여부, 추적검사의 종료 시점 등에 대해서는 관련 연구가 제한적이라 더 많은 장기간 데이터들이 보고되기 전까지는 결론짓기 어려워 보인다.
4. CNPH에서 발견된 양성 소견의 관리
CNPH 환자에서 MRCP-S 혹은 EUS를 통해 확인되는 췌장의 형태학적 변화는 50%에서 60% 사이의 범위를 가지나[ 25- 27, 30, 37, 38], 그 장기간 추적관찰의 데이터가 제시되지 않은 상태로 임상적 의의는 확실히 알려지지 않았다. 악성 질환의 경우 임상적 의의는 논란의 여지가 없을 것이며, 양성 질환 중 수술이나 주기적인 추적관찰이 필요할 가능성이 있는 병변인 IPMN을 비롯한 PCLs, 그 외 췌장종양, 만성 췌장염 등의 경우 임상적 의미를 가진다고 보여지나 그 외의 이상소견들은 그렇지 못하다[ 39]. 이러한 이상소견들의 진단율은 CNPH 환자군과 대조군을 비교하는 연구 그 의의를 확인해볼 수 있다. Mortele 등[ 38]의 연구에서는 분할췌, 췌장의 낭성병변, 정상 췌장이 CNPH군에서 대조군에 비해 더 많이 보고되었고 악성 병변은 대조군에서만 보고되었다. Testoni 등[ 25]의 연구에서는 MRCP-S에서 이상소견이 발견되는 비율이 CNPH군과 대조군에서 각각 52%와 7.1%로 확연한 차이를 보였다. Di Leo 등[ 37]의 연구에서는 EUS에서 정상으로 관찰되는 비율이 CNPH군과 대조군에서 각각 39.7%와 86.8%로 의미 있는 차이를 보였다. 따라서 CNPH군에서의 이상소견을 발견하기 위해 적극적인 검사를 시행하는 것은 어느 정도 타당성을 가진다고 보여진다. 임상적으로 의미를 가지는 양성 소견들은 CNPH 환자의 평가 중 상당수 발견된다. 췌관 확장은 MRCP-S로 검사를 하게 되는 경우 더욱 잘 확인할 수 있게 되는데, 특히 기존 MRCP에 비해서 측분지의 확장을 더욱 확실히 관찰할 수 있다(63% vs. 5%) [ 40]. 췌장의 낭성병변의 진단율은 MRCP나 EUS를 통해서 10-27.5% 정도로 진단되며[ 25- 27, 37], 만성 췌장염은 EUS를 이용하는 것이 진단에 이점을 보이며 약 26% 정도로 보고되었다[ 30, 37].
1) 만성 췌장염
만성 췌장염이 있다면 증상 없이 효소 수치의 상승소견이 동반되기도 하는데, 효소 수치의 상승 정도와 질환의 중증도와는 무관하며, 이들 중 상당수가 급성 악화가 아닌 macroamylasemia 때문이라는 연구 결과도 있기에 효소 수치 상승에 대해서는 해석에 주의를 기울어야 한다[ 41]. 조기에 발견되는 경증의 췌장 변화가 환자의 임상적인 결과나 예후에 미치는 영향에 대해서는 정확히 알려져 있는 바가 없다. 췌장질환이나 과도한 알코올 섭취가 없었던 평균 나이 66세인 환자들의 부검 결과 15% 정도에서 중등도-중증의 췌장 섬유화가 보고된 바 있다[ 42]. 따라서 노화 과정으로 자연스럽게 관찰되는 췌장의 이상소견을 검사를 통해 확인하는 것일 수도 있다. Di Leo 등[ 37]의 연구에서는 통계적으로 유의미하게 나이가 많은 환자에서 이상소견이 많이 확인되었고(50.6세 vs. 61.4세, P = 0.007), Antonini 등[ 43]의 연구에서는 이상소견이 없는 경우 평균 나이가 62.7세였으나 만성 췌장염의 경우 50.6세였다. 이에 대해서 결론을 내리기 위해서는 경증의 만성 췌장질환자에 대한 장기간 추적관찰 결과가 제시되어야 할 것이다.
2) IPMN과 췌장 낭성병변
기존 CNPH 환자를 대상으로 한 연구들에서 췌장의 낭성병변의 경우 27.5%까지 발견되는 것으로 보고되었고 모두 크기가 1 cm 이하의 병변들로 보고되었으며, IPMN의 진단율을 따로 제시한 연구들을 살펴보면 6.7-14.7% 정도로 확인된다[ 28, 30, 43]. 최근 한 연구에 따르면 분지췌관형 IPMN의 5%에서 무증상 췌장효소 상승이 최초로 보고되는 특징이라는 보고가 있다[ 44]. BD-IPMN의 경우는 악성 가능성이 12-47% 정도이며[ 45], 변화 양상에 대해 추적관찰이 필요하다. 한 연구에서 수술적 절제술을 시행받은 IPMN 환자들을 대상으로 분석하였을 때, 췌장효소의 상승이 invasive IPMN 및 췌장암과 양의 상관관계를 가진다고 하고 있으나 이들은 수술을 시행한 환자를 대상으로 한 제한적인 연구이다[ 46]. Pezzilli 등[ 47]의 연구에 따르면 췌장효소의 상승의 정도가 만성 췌장염이나 췌장의 낭성병변 그리고 췌장암에서 의미 있는 차이를 보이지 않았기에 낭성병변에서의 이러한 췌장효소의 상승은 비특이적인 소견으로 생각된다. 이러한 IPMN이나 낭성병변은 일부 췌장염을 발생시킬 수 있어 췌장효소의 상승의 원인이 될 수는 있으나 그 관계가 명확한 것은 아니며, 낭성병변에 대해서는 추천되는 가이드라인에 따라 추적관찰을 하는 것이 필요하겠다.
3) 분할췌와 delayed main pancreatic duct emptying
분할췌의 경우 일반 인구에서 2.9-22% 정도의 유병률을 가진다고 알려진 가장 흔한 췌장의 선천적 기형인데, 동양에서는 서양에 비해 그 유병률이 낮게 보고된다[ 48- 50]. CNPH 환자를 대상으로한 연구에서 발견되는 분할췌의 진단율은 3.1-27.5% 정도로 기존에 알려진 유병률에서 크게 벗어나지는 않지만 비교적 많이 진단된다고 생각된다[ 25, 26, 28, 37, 38, 51]. 분할췌의 경우 반복적인 복통의 원인이 될 수 있고[ 32], 급성 혹은 만성 췌장염 등을 일으킬 수 있다[ 52]. 하지만 증상을 일으키는 경우가 아니라면 특별한 예방적 조치가 필요하지는 않다. Delayed main pancreatic duct emptying은 오디괄약근의 기능이상을 시사하는 소견이라고 볼 수 있으며, 오디괄약근의 기능이상의 유병률은 1.5% 정도로 보고되고 있다[ 53]. 오디괄약근의 기능이상의 진단기준에 맞지 않는 delayed main pancreatic duct emptying 소견은 임상적으로 큰 의미를 가지는 것은 아니며 치료의 대상으로 보기도 어렵다. 분할췌나 오디괄약근 기능이상과 같은 이상이 동반되는 경우 췌액이 분비되는 것이 어려워질 수 있어 췌장효소 상승의 원인이 될 수 있으리라고는 생각된다. 분할췌의 경우 Di Leo 등[ 37]의 연구에서는 대조군에 비해 큰 차이로 발견되었으며(16.1%, 1.5%), Testoni 등[ 25]의 연구에서는 복통을 호소하는 군과의 비교에서 비슷한 수준으로 진단되어 증상이 없는 경우에 있어서는 의미가 있다고 보여진다(8%, 3.6%). Delayed main pancreatic duct emptying의 경우는 Testoni 등[ 25]의 연구에서 비슷한 수준으로 보고되어(12%, 10.7%) 큰 차이를 보이지 않고 있어 췌장효소의 상승의 원인이라고 말할 근거가 빈약하다.
4) 췌관 확장
췌관의 확장이 관찰되는 환자에 대해서 추적관찰한 연구는 흔하지 않으며, 췌관의 확장에 대하여 정확한 정의가 있는 것은 아니다. 일반적으로 췌장 두부에서 3 mm보다 큰 경우, 체부나 미부에서 2 mm보다 큰 경우를 이야기하며 나이가 들면 췌관이 확장되지만 5 mm 이상 확장되는 경우는 드물다고 알려져 있다[ 29, 54]. 한 연구에서 담관확장이 없이 주췌관 확장만 있는 51명을 분석해본 결과 만성 췌장염(73%), 특발성 췌관확장(15%), 췌장암(4%), IPMN (4%) 등으로 보고된 바 있고 대부분은 양성질환으로 보고된 바 있다. 다만, 잘 알려진 것처럼 이 연구에서도 담관확장이 동반되는 경우 악성의 확률이 높아지는 것으로 확인되었기에 저자들은 담췌관 및 주췌관이 함께 확장되어있는 경우나, 주췌관 확장만 있으나 만성 췌장염의 증거가 없는 두 가지 경우에 악성의 가능성이 높다고 이야기하고 있다[ 55]. 또한, 약 1,058명을 대상으로 장기간 추적관찰을 한 연구에서 평균 75.5개월을 추적관찰 하여 12명이 췌장암이 발병하였고, 이 환자들을 분석한 결과 주췌관이 약간 확장된 소견이(≥ 2.5 mm) 이 췌장암을 예측하는 강한 예측인자로 평가되었고, 그 위험도는 6.38이었다[ 56]. 따라서 이러한 췌관확장이 발견되는 경우에 특발성이 아닌 이차성으로 동반되는 소견일 가능성이 있기에 주의 깊게 경과 관찰을 해야 할 것으로 생각되며 특히 만성 췌장염이 없거나 담관확장이 동반된 경우라면 더욱 주의 깊게 추적관찰 해야겠다.
결 론
최근 영상기술 및 진단검사의학기술의 발달 및 시행증가로 각종 췌담도질환의 진단율이 높아지고 있으며 환자를 진료하는 현장에서는 그 임상적 의미에 대한 적절한 해석이 매우 중요해지고 있다. 아밀라아제와 리파아제로 대표되는 췌장효소의 상승이 확인된 환자에 대해서는 처음 철저한 병력청취가 중요하며, 가장 먼저 췌장염을 감별하고, 췌장염이 없다면 췌장효소의 신배설이 저하되는 상태나, 복강내 다른 문제, 전신질환, 약물, 췌장의 구조적 이상, CNPH 등에 대한 고려가 필요하다. CNPH가 의심되는 경우 복부 초음파나 CT에서 이상소견이 없더라도, MRCP나 EUS 등의 추가검사를 적극 시행하여 연관된 췌장의 이상소견을 충분히 확인하는 것이 바람직하겠고 동반된 소견에 맞추어 추적관찰 및 치료에 대해서 개별화 하여 접근해야겠다. 현재까지 보고된 연구들만으로 CNPH 환자에서 시행해야 할 검사의 범위나 동반된 소견의 추적관찰에 대해 결론 내리기에는 무리가 있어 향후 대규모 장기간 추적관찰 연구가 필요할 것으로 보인다.
REFERENCES
1. Frulloni L, Patrizi F, Bernardoni L, Cavallini G. Pancreatic hyperenzymemia: clinical significance and diagnostic approach. JOP 2005;6:536-551.  2. Matteucci E, Giampietro O. Diabetes and pancreas: why so difficult? Potential mechanisms of elevated serum pancreatic enzymes. Curr Med Chem 2016;23:290-302.   3. Tietz NW, Shuey DF. Lipase in serum--the elusive enzyme: an overview. Clin Chem 1993;39:746-756.  4. Terada T, Kida T, Nakanuma Y. Extrahepatic peribiliary glands express alpha-amylase isozymes, trypsin and pancreatic lipase: an immunohistochemical analysis. Hepatology 1993;18:803-808.   5. Collen MJ, Ansher AF, Chapman AB, Mackow RC, Lewis JH. Serum amylase in patients with renal insufficiency and renal failure. Am J Gastroenterol 1990;85:1377-1380.  6. Pezzilli R, Andreone P, Morselli-Labate AM, et al. Serum pancreatic enzyme concentrations in chronic viral liver diseases. Dig Dis Sci 1999;44:350-355.   7. Kemppainen EA, Hedström JI, Puolakkainen PA, et al. Rapid measurement of urinary trypsinogen-2 as a screening test for acute pancreatitis. N Engl J Med 1997;336:1788-1793.   8. Steinberg WM, Goldstein SS, Davis ND, Shamma'a J, Anderson K. Diagnostic assays in acute pancreatitis. A study of sensitivity and specificity. Ann Intern Med 1985;102:576-580.   10. Shah AM, Eddi R, Kothari ST, Maksoud C, DiGiacomo WS, Baddoura W. Acute pancreatitis with normal serum lipase: a case series. JOP 2010;11:369-372.  11. Yadav D, Agarwal N, Pitchumoni CS. A critical evaluation of laboratory tests in acute pancreatitis. Am J Gastroenterol 2002;97:1309-1318.   12. Sachdeva CK, Bank S, Greenberg R, Blumstein M, Weissman S. Fluctuations in serum amylase in patients with macroamylasemia. Am J Gastroenterol 1995;90:800-803.  13. Eleccion CB, Hathaway AA. Macroamylasemia in HIV infection. Tex Med 1998;94:77-79.  14. Rabsztyn A, Green PH, Berti I, Fasano A, Perman JA, Horvath K. Macroamylasemia in patients with celiac disease. Am J Gastroenterol 2001;96:1096-1100.   15. Van Gossum A, Cremer M. Macroamylasemia disappearance after gluten withdrawal. Dig Dis Sci 1989;34:964-966.  16. Borovickova I, Bhatt NR, Boran GP, Ridgway PF. Persistent chronic hyperamylasemia: clinical interpretation and diagnostic approach. JOP 2016;17:349-358.
17. Hameed AM, Lam VW, Pleass HC. Significant elevations of serum lipase not caused by pancreatitis: a systematic review. HPB (Oxford) 2015;17:99-112.   18. Malloy J, Gurney K, Shan K, Yan P, Chen S. Increased variability and abnormalities in pancreatic enzyme concentrations in otherwise asymptomatic subjects with type 2 diabetes. Diabetes Metab Syndr Obes 2012;5:419-424.   19. Duerksen DR, Tsang M, Parry DM. Chronic hyperlipasemia caused by sarcoidosis. Dig Dis Sci 2000;45:1545-1548.   20. Warshaw AL, Lee KH. Macroamylasemia and other chronic nonspecific hyperamylasemias: chemical oddities or clinical entities? Am J Surg 1978;135:488-493.   21. Gullo L. Benign pancreatic hyperenzymemia. Dig Liver Dis 2007;39:698-702.   22. Gullo L. Day-to-day variations of serum pancreatic enzymes in benign pancreatic hyperenzymemia. Clin Gastroenterol Hepatol 2007;5:70-74.   23. Gullo L. Familial pancreatic hyperenzymemia. Pancreas 2000;20:158-160.   24. Gullo L. Chronic nonpathological hyperamylasemia of pancreatic origin. Gastroenterology 1996;110:1905-1908.   25. Testoni PA, Mariani A, Curioni S, Giussani A, Masci E. Pancreatic ductal abnormalities documented by secretin-enhanced MRCP in asymptomatic subjects with chronic pancreatic hyperenzymemia. Am J Gastroenterol 2009;104:1780-1786.   26. Donati F, Boraschi P, Gigoni R, et al. Secretin-stimulated MR cholangiopancreatography in the evaluation of asymptomatic patients with nonspecific pancreatic hyperenzymemia. Eur J Radiol 2010;75:e38-44.   27. Amodio A, Manfredi R, Katsotourchi AM, et al. Prospective evaluation of subjects with chronic asymptomatic pancreatic hyperenzymemia. Am J Gastroenterol 2012;107:1089-1095.   28. Galassi E, Birtolo C, Migliori M, et al. A 5-year experience of benign pancreatic hyperenzymemia. Pancreas 2014;43:874-878.   30. Pezzilli R, Morselli-Labate AM, Casadei R, et al. Chronic asymptomatic pancreatic hyperenzymemia is a benign condition in only half of the cases: a prospective study. Scand J Gastroenterol 2009;44:888-893.   31. Zhang XM, Shi H, Parker L, Dohke M, Holland GA, Mitchell DG. Suspected early or mild chronic pancreatitis: enhancement patterns on gadolinium chelate dynamic MRI. Magnetic resonance imaging. J Magn Reson Imaging 2003;17:86-94.   32. Zhang XM, Mitchell DG, Dohke M, Holland GA, Parker L. Pancreatic cysts: depiction on single-shot fast spin-echo MR images. Radiology 2002;223:547-553.   33. de Jong K, Nio CY, Hermans JJ, et al. High prevalence of pancreatic cysts detected by screening magnetic resonance imaging examinations. Clin Gastroenterol Hepatol 2010;8:806-811.   34. Kimura W, Nagai H, Kuroda A, Muto T, Esaki Y. Analysis of small cystic lesions of the pancreas. Int J Pancreatol 1995;18:197-206.  35. Pascual I, Soler J, Peña A, et al. Morphological and functional evaluation of the pancreatic duct with secretin-stimulated magnetic resonance cholangiopancreatography in alcoholic pancreatitis patients. Dig Dis Sci 2008;53:3234-3241.   36. Czakó L. Diagnosis of early-stage chronic pancreatitis by secretin-enhanced magnetic resonance cholangiopancreatography. J Gastroenterol 2007;42 Suppl 17:113-117.   37. Di Leo M, Petrone MC, Zuppardo RA, et al. Pancreatic morphofunctional imaging as a diagnostic approach for chronic asymptomatic pancreatic hyperenzymemia. Dig Liver Dis 2016;48:1330-1335.   38. Mortelé KJ, Wiesner W, Zou KH, Ros PR, Silverman SG. Asymptomatic nonspecific serum hyperamylasemia and hyperlipasemia: spectrum of MRCP findings and clinical implications. Abdom Imaging 2004;29:109-114.   39. Frulloni L, Amodio A. Endoscopic ultrasonography in chronic asymptomatic pancreatic hyperenzymemia: the more we see, the less we know. Dig Liver Dis 2017;49:232-233.   40. Cappeliez O, Delhaye M, Devière J, et al. Chronic pancreatitis: evaluation of pancreatic exocrine function with MR pancreatography after secretin stimulation. Radiology 2000;215:358-364.   41. Gubergrits N, Golubova O, Lukashevich G, Fomenko P. Elevated serum amylase in patients with chronic pancreatitis: acute attack or macroamylasemia? Pancreatology 2014;14:114-116.   42. van Geenen EJ, Smits MM, Schreuder TC, van der Peet DL, Bloemena E, Mulder CJ. Smoking is related to pancreatic fibrosis in humans. Am J Gastroenterol 2011;106:1161-1166 quiz 1167.   43. Antonini F, Belfiori V, Pagano N, et al. Endoscopic ultrasonography may select subjects having asymptomatic chronic pancreatic hyperenzymemia who require a more strict follow-up. Pancreas 2017;46:524-527.   44. Pezzilli R, Calculli L. Branch-type intraductal papillary mucinous neoplasm of the pancreas: clinically and patient-reported outcomes. Pancreas 2015;44:221-226.   45. Stark A, Donahue TR, Reber HA, Hines OJ. Pancreatic cyst disease: a review. JAMA 2016;315:1882-1893.   46. Roch AM, Parikh JA, Al-Haddad MA, et al. Abnormal serum pancreatic enzymes, but not pancreatitis, are associated with an increased risk of malignancy in patients with intraductal papillary mucinous neoplasms. Surgery 2014;156:923-929.   47. Pezzilli R, Melzi d'Eril G, Barassi A. Can serum pancreatic amylase and lipase levels be used as diagnostic markers to distinguish between patients with mucinous cystic lesions of the pancreas, chronic pancreatitis, and pancreatic ductal adenocarcinoma? Pancreas 2016;45:1272-1275.   48. Liao Z, Gao R, Wang W, et al. A systematic review on endoscopic detection rate, endotherapy, and surgery for pancreas divisum. Endoscopy 2009;41:439-444.   49. Kim HJ, Kim MH, Lee SK, et al. Normal structure, variations, and anomalies of the pancreaticobiliary ducts of Koreans: a nationwide cooperative prospective study. Gastrointest Endosc 2002;55:889-896.   50. Kin T, Shapiro AM, Lakey JR. Pancreas divisum: a study of the cadaveric donor pancreas for islet isolation. Pancreas 2005;30:325-327.   51. Gullo L, Lucrezio L, Calculli L, et al. Magnetic resonance cholangiopancreatography in asymptomatic pancreatic hyperenzymemia. Pancreas 2009;38:396-400.   52. Levy MJ, Geenen JE. Idiopathic acute recurrent pancreatitis. Am J Gastroenterol 2001;96:2540-2555.   53. Small AJ, Kozarek RA. Sphincter of oddi dysfunction. Gastrointest Endosc Clin N Am 2015;25:749-763.   54. Glaser J, Stienecker K. Pancreas and aging: a study using ultrasonography. Gerontology 2000;46:93-96.   56. Tanaka S, Nakao M, Ioka T, et al. Slight dilatation of the main pancreatic duct and presence of pancreatic cysts as predictive signs of pancreatic cancer: a prospective study. Radiology 2010;254:965-972.  
Fig. 1.
Possible diagnostic algorithm in patients with pancreatic hyperenzymemia. Based on detailed medical history, physical examination, basic blood test, abdominal ultrasound, and simple radiography, the possibility of acute pancreatitis, impaired excretion of pancreatic enezyme and adverse reaction of drug should be excluded. Subsequent exclusion of additional pancreatic or nonpancreatic causes via tumor markers, isoenzymes, ACCR/PEG precipitation test, and abdominal CT. If pancreatic enzyme elevation is confirmed during repeated tests and there is no specific abnormal finding for EUS or MRCP, CNPH may be diagnosed and should be followed-up appropriately. CBC, complete blood count; USG, ultrasonography; ACCR/PEG, amylase-to-cre atinine clearance ratio/polyethylene glycol; CT, computed tomography; MRCP, magnetic resonance cholangiopancreatography; EUS, endoscopic ultrasonography; CNPH, chronic non-pathological pancreatic hyperenzymemia. 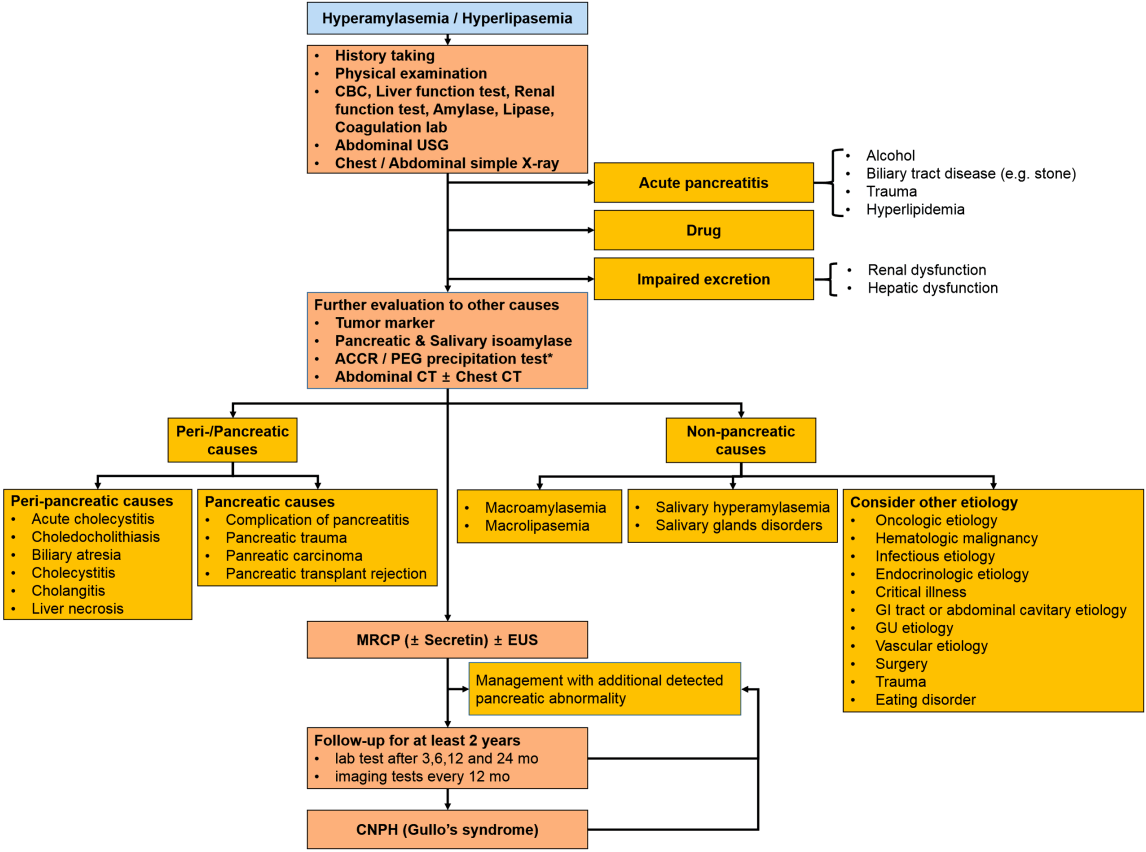
Table 1.
Possible causes of hyperamylasemia or hyperlipasemia [ 16, 17]
|
Etiology of hyperamylasemia |
|
Hyperamylasemia associated with abdominal pain |
|
Pancreatic disorder |
|
Pancreatitis of any etiology: alcohol, biliary tract disease, trauma, hyperlipidemia |
|
Complications of acute pancreatitis: pancreatic abscess, pseudocyst, ascites, pleural effusion |
|
Pancreatic trauma (blunt trauma, abdominal/retroperitoneal surgery, endoscopic retrograde cholangiopancreatography) |
|
Pancreatic cancer |
|
Non-pancreatic gastrointestinal tract / vascular conditions |
|
Acute cholecystitis, choledocholithiasis |
|
Gastritis, duodenitis, gastroenteritis, peptic ulcer |
|
Inflammatory bowel disease |
|
Intestinal obstruction |
|
Peritonitis |
|
Dissecting/Ruptured abdominal aortic aneurysm |
|
Mesenteric infarction |
|
Abdominal trauma |
|
Non-pancreatic genitourinary conditions |
|
Urolithiasis |
|
Endometriosis, salpingitis |
|
Ectopic/ruptured tubal pregnancy |
|
Hyperamylasemia associated with salivary gland disorders |
|
Chronic alcoholism |
|
Anorexia nervosa/Bulimia |
|
Duct obstruction/Caliculi |
|
Sjögren’s syndrome |
|
Mumps |
|
Trauma, surgery |
|
Injection of constrast medium into salivary ducts for sialography |
|
Miscellaneous causes |
|
Tumors: carcinoma of lung, ovary, breast, renal cell, colon, thymoma, multiple myeloma, hematologic malignancies, pheochromocytoma |
|
Renal failure |
|
Liver disease: hepatitis, liver cirrhosis, hepatocellular carcinoma |
|
Acute alcoholic abuse |
|
Diabetic ketoacidosis and non-ketotic acidosis |
|
Post-surgery: pancreatic, abdominal, hepatic, biliary, cardiovascular, post-ERCP, liver transplantation |
|
Macroamylasemia |
|
Acute myocardiac infarction |
|
Acquired immune deficiency syndrome |
|
Acute porphyria |
|
Glycogen storage disease type 1 |
|
Drugs: anti-retroviral agents (atazanavir, cidofovir, enfuvirtide, foscarnet, indinavir, lamivudine, zidovudine), azathioprine, clozapine, cyclosporine, didanosine, sphedrine, oral contraceptives, paracetamol, pentamidine, propofol, ritodrine, roxithromycin, steroids, tamoxifen |
|
Reduced clearance/physiological |
|
Renal impairment |
|
Macrolipase: presence of macrolipase may sometimes indicate an increased risk for associated disorders, such as autoimmune or lymphoproliferative disease |
|
Intra-abdominal pancreatic and non-pancreatic causes (other than pancreatitis) |
|
Inflammation: in adjacent organs/structures to pancreas such as biliary tranct and gastrointestinal tract |
|
Obstruction: biliary, pancreatic duct or bowel obstruction |
|
Alternative sources of lipase: stomach, small bowel, liver, gallbladder and other surrounding organs may potentially act as non-pancreatic sources of lipolytic enzymes |
|
Peritonitis |
|
Impaired hepatic function: chronic liver diseas, biliary atresia etc. |
|
Neoplasia: may be related to biliary or pancreatic ductal obstruction, macrolipase, or functional tumor mass |
|
Non-pathological pancreatic hyperenzymemia |
|
Critical illness |
|
Intensive care unit patients with critical illness or multi-organ failure |
|
Neurosurgical patients with severe head injuries |
|
Some alternative causes: diabetic ketoacidosis and type I diabetes mellitus |
|
Drugs: alcohol, morphine with prostigmine provocation, sorafenib (?), nilotinib (?), dipeptidyl-peptidase-4 inhibitors (?) |
Table 2.
Imaging findings in studies on asymptomatic subjects with chronic pancreatic hyperenzymemia
|
Author (year) |
Modality |
N |
Normal |
Benign
|
Malignancy |
|
CP |
PCLs |
Ductal dilatation |
Pancreas divisum |
Delayed MPD emptying |
Etc |
|
Mortelé et al (2004) [38] |
MRCP |
54 |
23 (42.6) |
9 (16.7) |
7 (13) |
- |
10 (18.5) |
- |
5 (9.5) |
- |
|
Gullo et al (2009) [51] |
MRCP |
63 |
57 (90.5) |
- |
2 (3.1) |
1 (1.6) |
2 (3.1) |
- |
1 (1.6) |
- |
|
Testoni et al (2009) [25] |
MRCP |
25 |
20 (80) |
- |
2 (8.0) |
2 (8.0) |
2 (8.0) |
- |
- |
- |
|
MRCP-S |
25 |
12 (48) |
- |
2 (8.0) |
13 (52) |
2 (8.0) |
3 (12) |
- |
- |
|
Pezzilli et al (2009) [30] |
MRCP, EUS |
75 |
31 (41.3) |
20 (26.7) |
8 (10.7) |
- |
- |
- |
13 (17) |
3 (4.0) |
|
Donati et al (2010) [26] |
MRCP |
80 |
40 (50) |
2 (2.5) |
24 (30.0) |
- |
12 (15.0) |
- |
4 (5.1) |
- |
|
MRCP-S |
80 |
25 (31.3) |
14 (17.5) |
22 (27.5) |
- |
22 (27.5) |
- |
4 (5.1) |
- |
|
Amodio et al (2012) [27] |
MRCP |
160 |
117 (73.1) |
- |
4 (2.5) |
34 (21.3) |
- |
- |
7 (4.3) |
1 (0.6) |
|
MRCP-S |
160 |
80 (50) |
- |
4 (2.5) |
MPD |
- |
23 (14) |
10 (6.1) |
|
|
|
|
|
|
44 (26.3) |
|
|
|
|
|
|
|
|
|
BD |
|
|
|
|
|
|
|
|
|
58 (36.2) |
|
|
|
|
|
Galassi et al (2014) [28] |
MRCP |
183 |
168 (91.8) |
- |
8 (4.4) |
- |
6 (3.3) |
- |
1 (0.5) |
- |
|
EUS |
68 |
27 (39.7) |
22 (32.4) |
10 (14.7) |
- |
11 (16.1) |
- |
1 (1.5) |
- |
|
MRCP-S |
68 |
33 (48.5) |
14 (20.6) |
6 (8.9) |
- |
12 (17.7) |
4 (5.9) |
|
- |
|
Antonini et al (2017) [43] |
MRCP, EUS |
45 |
38 (84.4) |
1 (2.2) |
1 (2.2) |
- |
1 (2.2) |
- |
1 (2.2) |
- |
|
|













