서 론
수술이 불가능한 진행성 췌장암, 담도암 및 담낭암 환자에서 현재 국내에서 사용중인 1차 항암 화학 요법은 FOLFIRINOX(5-fluorouracil+leucovorin+oxaliplatin+irinotecan), gemcitabine+ nanoparticle albumin-bound paclitaxel (nab-paclitaxel), 및 gemcitabine+cisplatin이다[1-3]. 2019년 National Comprehensive Cancer Network (NCCN) guideline은 췌장암 환자의 경우, 전신 상태가 양호할 때(Eastern Cooperative Oncology Group [ECOG], good biliary drainage, nutritional intake) 우선 clinical trial 등록 및 항암 치료를 권고한다[4]. 진행성 췌장암, 담도계암 환자에서 항암 화학 요법을 시행하는 이유는 다음과 같다. 첫째, 종양 크기의 감소 및 성장의 억제, 둘째, 혈관 내 미세 암세포의 파괴, 셋째, 타 장기로 암세포의 전이 방지, 넷째, 통증을 비롯한 암 유발 증상의 최소화, 다섯째, 방사선 치료 및 기타 생물학적 치료 효과를 극대화하기 위함이다. 실제 fluorouracil 기반의 항암 화학 요법은 지지 요법(supportive care) 단독과 비교하여 대략 3개월의 전체 생존 기간을 개선시켰으며, 2차 항암요법의 경우에도 단순 지지 요법에 비하여 OFF regimen (oxaliplatin, 5-FU, and folinic acid)의 경우, 통계적으로 유의한 생존율 상승을 보여 주었다(second line survival, 4.8 months vs. 2.3 months, p=0.008) [5,6]. 본고에서는 진행성 췌장암, 담도계암 환자에서 언제 항암 치료를 시작할 것인지, 치료 반응 평가의 적절한 방법 및 시기에 대하여 알아보고, 마지막으로 항암 치료를 중단하는 시점에 대하여 최신 문헌이나 지금까지 발표된 가이드라인을 통하여 알아보고자 한다.
본 론
1. 항암 화학 요법의 시작
1) 항암 화학 요법의 시작 요건
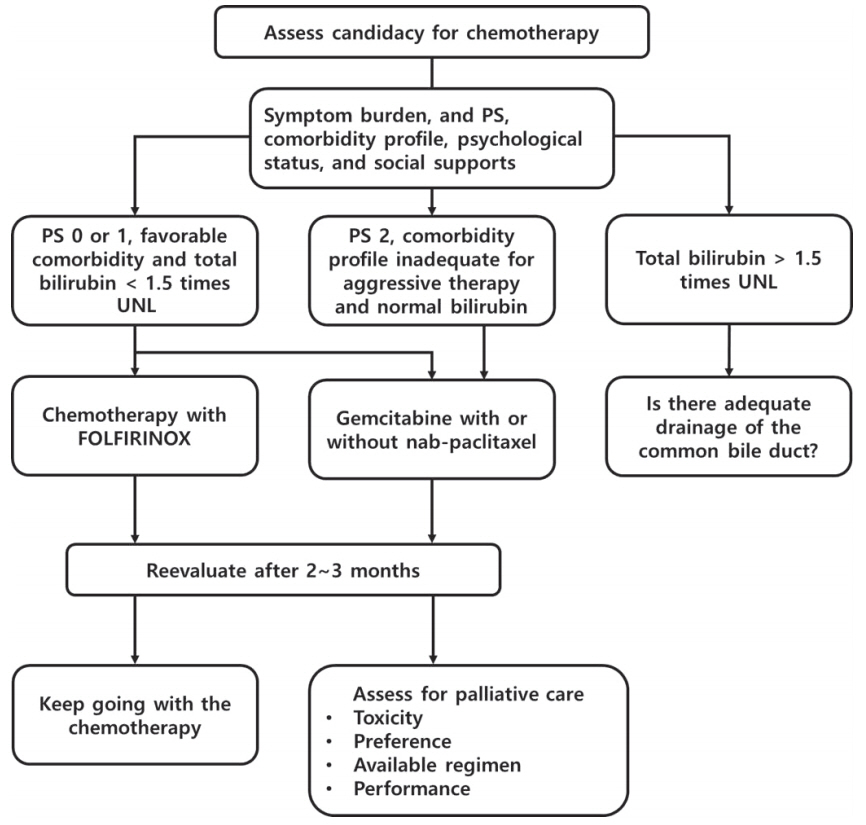
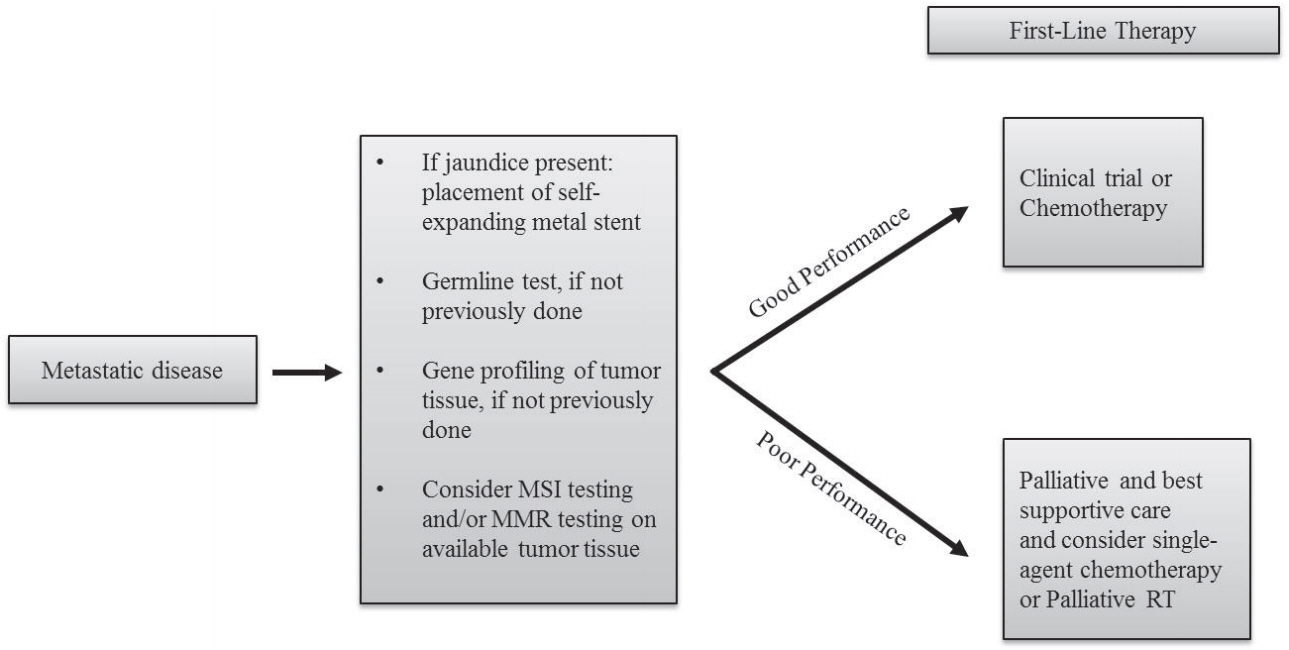
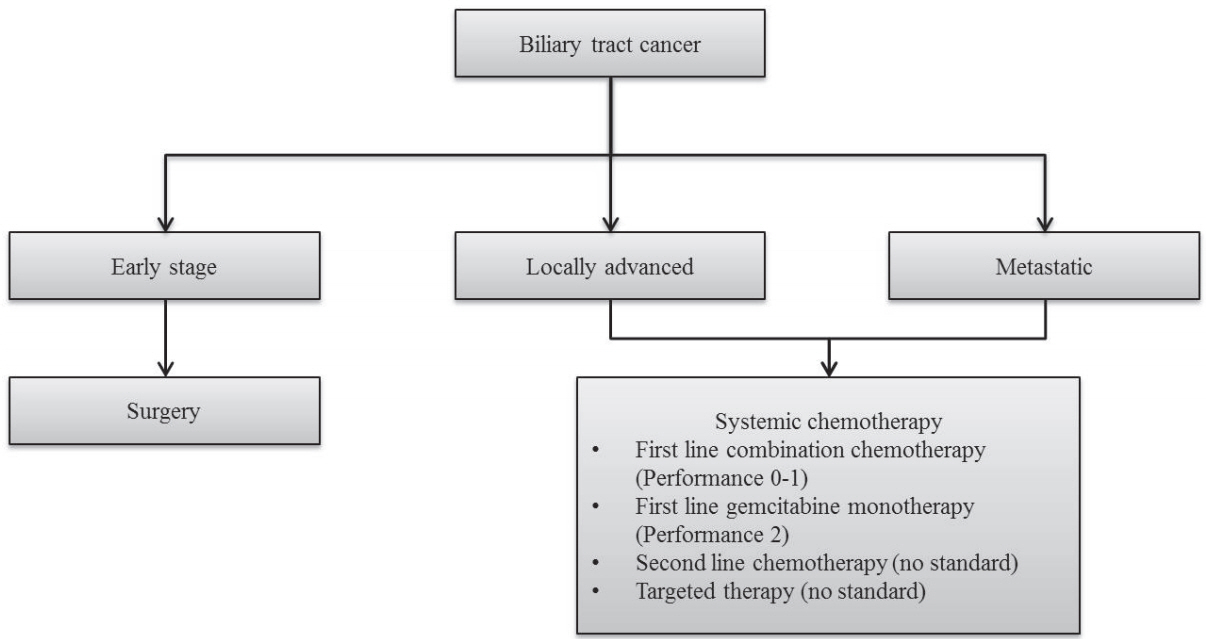
항암 화학 요법의 시작을 결정하는 데 영향을 미치는 요인은 증상의 유무, performance status, 합병된 동반 질환 유무, 현재 사용 가능한 치료 옵션 유무 그리고 환자의 항암에 대한 선호 여부 등이다. 처음 환자가 내원하면 기본 performance status, 증상, 정신과적 문제 등을 상담해야 한다. NCCN 가이드라인 (Fig. 1)은 good performance를 보이는 경우, 항암 치료의 시작을 권고하며, good performance의 정의는 ECOG 0-1, good biliary drainage, adequate nutritional intake (단, gemcitabine+albuminbound paclitaxel을 고려 중이라면 ECOG 0-2)와 같다[4]. American Society of Clinical Oncology (ASCO) 가이드라인에 따르면 comorbidity profile에 따라 항암치료의 시작을 권고하고 있고 Table 1과 같다[7]. 유럽 가이드라인에 따르면 FOLFIRINOX 항암 화학 요법의 경우, 75세 미만의 good performance status (0-1)를 보이고, 총 빌리루빈값이 정상 상한치의 1.5배 미만인 경우에 사용을 권고한다. 담도암 및 담낭암의 경우, 2016년 European Society for Medical Oncology 가이드라인에서 performance 0-1은 combination chemotherapy를 그리고 performance 2 환자에서는 gemcitabine 단독 요법을 권고하고 있다(Fig. 2) [8].
특히, 췌장암 및 담도암의 경우, 진단 시점에 담도 폐색이 동반된 경우가 많고, 항암 화학 요법 시작 전 황달의 해결이 필수적이다. 가이드라인에서는 진단 시점에 황달이 동반된 경우, 스텐트 삽입을 통한 담즙 배액을 치료 전 권고한다. 항암 화학 요법 시작 전 담도 폐색을 해결하는 가장 큰 이유는 간독성으로 인한 간부전을 방지하기 위함이다. 대표적인 항암 약제인 gemcitabine과 5-fluorouracil로 크게 나누어 기존 연구 결과들을 살펴보면 다음과 같다. 5-fluorouracil의 경우, 10% 만이 소변을 통하여 배설되고, 나머지는 간에서 dihydropyrimidine dehydrogenase에 의하여 대사된다. 그래서 정맥 정주 5-fluorouracil의 간에서 대사 역할 때문에 일부 연구에서는 총 빌리루빈이 5 mg/dL 이상인 경우, 항암 약제 투여를 제한한다[9]. Gemcitabine의 경우, 총 빌리루빈 1.6 mg/dL 미만을 치료 요건으로 권고하고 있으나, 일부 연구에서는 총 빌리루빈 4.5 mg/dL 이상에서도 full dose gemcitabine이 부작용 없이 안전하게 투여 가능함을 보고하였다. 최근 European Journal of Cancer에 발표된 보고에 따르면 황달이 있는 환자에서 gemcitabine+nab-paclitaxel을 사용하는 경우, 추가적인 간독성 및 혈액 독성을 유발하지 않음을 보여주었다. 이는 심지어 총 빌리루빈이 5 mg/dL 이상인 환자도 포함한 연구이다[10-12]. 하지만 아직까지 미국과 유럽의 가이드라인에서는 담도 배액을 통하여 총 빌리루빈이 정상 상한치의 1.5배 미만(또는 2 mg/dL 미만)에서 항암 화학 요법을 시작하기를 권고하고 있다.
2) 항암 화학 요법의 시작 시점
췌장암 및 담도암의 경우, 수술 후 항암 화학 요법의 시작 시점에 관한 연구는 일부 있으나, 전이성 췌장암 및 담도암에서 1차 항암 화학 요법의 시작 시점에 관한 연구는 드물다. 2016년에 발표된 종설에 의하면, 저자들은 대장암을 포함한 6개 암종에 대하여 항암 화학 요법의 시작 시점과 환자의 예후간 상관관계를 분석하였고 8주 미만과 비교하여 진단 후 8주 이상 지나 항암 화학 요법이 시작되는 경우, hazard ratio (HR)가 약 1.2배 증가함을 보였다(HR for death 1.20, 95% confidence interval 1.15-1.26) [13,14]. 하지만 1개월 미만, 1-2개월 그리고 2-3개월을 비교한 경우, 통계적으로 유의한 차이를 보이지는 않았다. 현재 NCCN, ASCO 가이드라인에서는 진단 후 최대 4주 이내에 항암 화학 요법의 시작을 권고한다.
2. 반응 평가
항암 화학 요법의 치료 반응 평가 시기는 NCCN, ASCO, European Society for Medical Oncology [15] 가이드라인에서 2-3개월 간격의 반응 평가를 권고하고, 이는 항암 약제의 종류와 치료 스케줄에 따라 변동 가능함을 보여준다. 고형 악성 종양의 반응 평가 방법으로는 전통적으로 크게 World Health Organization criteria (1981), response evaluation criteria in solid tumors (RECIST) criteria가 있다. 최근 다양한 암종에서 면역 항암제 사용이 증가하면서 immune-related response criteria (iRECIST or imRECIST)와 같은 새로운 평가 방법이 논의 중이나 정립되지는 않은 실정이다[16]. 국내의 경우, 췌장암 및 담도암 환자에서 사용 가능한 면역 항암제의 종류가 극히 제한적이고 면역 관련 치료 반응 평가 시스템의 기준이 확립되지 않아 기존의 항암 반응 평가 시스템을 사용 중이다. World Health Organization 정의를 사용할 경우, 종양의 크기 변화를 적절히 평가할 수 없다는 단점때문에 RECIST에서는 표적 및 비표적 병변들 모두에서 치료 반응을 평가한 뒤, 이를 바탕으로 전체적인 치료 반응 평가를 권고하고 있다. RECIST Criteria ver. 1.1 (2009) [17] 따른 치료 반응 평가 기준은 다음과 같다. 1) 완전 관해, complete response (CR): 병변 소실, 2) 부분 관해, partial response (PR): 장축의 합이 30% 이상 감소, 3) 불변, stable disease (SD): PR과 PD의 중간 단계, 4) 진행, progressive disease (PD): 장축의 합이 20% 이상 증가 혹은 새로운 병변 발생. 영상학적인 항암 화학 요법의 지속 요건은 CR, PR, SD이고 영상학적인 항암 화학 요법의 중단 조건은 PD이다. Measurable lesion은 길이를 잴 수 있는 병변으로 computed tomography 에서는 장축이 10 mm 이상이고 lymph node의 경우는 단축 기준 15 mm 이상을 일컫는다. Non-measurable lesion은 길이 측정이 어려운 병변으로 그 예로 뼈 전이, 흉수, 복막암종이 있다. 또, 장축 기준 10 mm 이하의 병변도 non-measurable lesion으로 일컫는다. Target 병변은 measurable lesion 중 최대 5개, 장기 당 2개까지 측정하여 합을 계산한다. 이 외는 nontarget lesion이다.
3. 항암 화학 요법의 중단
항암 화학 요법 중단의 이유는 크게 약제 독성으로 인한 경우와 환자의 전신 상태 악화에 따른 중단으로 나눌 수 있다. Cho 등[18]이 발표한 전이성 췌장암 환자를 대상으로 진행한 연구에서는 gemcitabine+nab-paclitaxel 사용 후 21%의 환자가 약제 독성으로 항암제 사용을 중단하였다. 췌장암의 경우, 일부 연구에서는 환자가 전신 상태 악화로 ECOG performance 3점 이상, second line 항암 화학 요법 후 progression 소견을 보이는 경우, 항암 화학 요법의 지속 여부를 상의할 것을 권고한다[19,20]. 주치의는 항암 치료의 중단 시기 결정과 관련해서 아래 문제들에 대한 지속적인 고민이 필요하다.
Question being asked
- Is the clinical benefit worth it? When the benefits are small, or toxicities are large.
- Is it time to switch to hospice-based care? Small benefit, or decreasing performance status.
- Is the patient having trouble paying for treatment? Depends on insurance coverage.
- Is the patient feeling a burden on the caregivers? Increasing disability and care needs.