Basic/Translational research
Review Article Korean J Pancreas Biliary Tract 2021; 26(4): 254-259. Published online: October 31, 2021 담관세포에서 담즙산 수용체의 역할
박진명1, 2
Bile Acid Receptors in Cholangiocyte
Jin Myung Park1, 2
1Department of Internal Medicine, Kangwon National University School of Medicine, Chuncheon, Korea 2Department of Internal Medicine, Kangwon National University Hospital, Chuncheon, Korea Corresponding author : Jin Myung Park Department of Internal Medicine, Kangwon National University Hospital, 156 Baengnyeong-ro, Chuncheon 24289, Korea Tel. +82-33-258-9235 Fax. +82-33-258-2404 E-mail; youreon.park@gmail.com
Copyright © 2021 by The Korean Journal of Pancreas and Biliary Tract This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits unrestricted noncommercial use, distribution, and reproduction in any medium, provided the original work is properly cited. 요약담즙산은 지방의 소화를 돕고 담즙의 배출을 용이하게 하는 역할을 하는 것으로 알려져 있었다. 하지만 여러 연구를 통해 담즙산에 대한 수용체가 존재하며 그 종류도 다양함을 알게 되었다. 담즙산 수용체는 담즙산 생리에 관여하는 것 외에도 에너지 대사, 염증 조절 등의 반응에 있어 인체 내에서 광범위하게 작용한다. GPBAR1과 S1PR2는 담즙산 수용체 중에서도 대표적인 G 단백질 결합수용체로서 담관세포에 많이 존재하며 세포의 증식 및 담즙 분비 등에 관여한다. 아울러 담관암의 진행과도 관련되어 있다는 연구가 발표되고 있어 향후 담관암 치료에 중요한 표적이 될 것으로 예상된다.
AbstractBile acids are known to play a role in helping the digestion of lipid and maintenance of the bile flow. However, since the first bile acid receptor was discovered in 1999, it has been found that various bile acid receptors are present. Bile acid receptors are involved in bile acid physiology, energy metabolism, and inflammatory response. G-protein bile acid-activated receptor 1 (GPBAR1) and Sphingosine-1-phosphate receptor 2 (S1PR2) are representative bile acid receptors in cholangiocyte. They are involved in proliferation and secretion of cholangiocyte, which seem to protect cholangiocyte from the toxicity of bile acids. GPBAR1 and S1PR2 are also associated with the progression of cholangiocarcinoma.
Keywords: Bile acids and salts, GPBAR1 protein, human, S1PR2 protein, human, Cholangiocarcinoma 서 론담즙산은 담즙의 주요 구성 성분으로서 간에서 생성되어 장관 내로 배출되며 장관 내에서 지질과 미셀(micelle)을 형성하여 지질의 체내 흡수를 보조하는 것으로 잘 알려져 있다. 그리고 담즙의 흐름을 유지하고 담즙 내에서 콜레스테롤이 용해된 상태로 존재하도록 돕는다. 그래서 오래 전부터 우르소데옥시콜산(ursodeoxycholic acid)이나 케노데옥시콜산(chemodeoxycholic acid) 등의 담즙산이 콜레스테롤 담석의 치료에 사용되었다.
담즙산에 대해 여러 가지 연구가 진행되면서 지방의 소화를 돕고 담즙의 배출을 용이하게 하는 것 외에도 또다른 역할을 한다는 것이 밝혀졌다. 1999년은 담즙산에 대한 획기적인 연구 결과가 발표된 시점인데, 서로 다른 세 개의 연구진이 일차담즙산은 farnesoid X 수용체(farnesoid X receptor, FXR)를 활성화시킬 수 있다고 보고하였다[1-3]. 초기에는 FXR이 단순히 담즙산을 감지하는 역할을 하는 것으로 생각하였으나 후속 연구를 통해 간 및 장관 세포에서 담즙산의 흡수, 간에서의 대사와 배출, 신장에서의 대사 등 담즙산 생리에 전반적으로 관여함이 알려졌다. 이후 FXR 외에 다양한 담즙산 수용체가 발견되었고 담즙산이 여러 수용체에 결합하여 지방과 포도당 등의 에너지 대사, 염증 조절, 장내 미생물의 성장 등 인체 내에서 광범위한 신호전달 호르몬으로서 작용을 한다는 것이 알려졌다[4].
담즙산 수용체는 크게 핵에 존재하는 수용체(neuclear receptor)와 세포막에 존재하는 수용체(cell membrane receptor)로 분류한다(Table 1). FXR은 최초로 발견된 담즙산 수용체로서 많은 연구가 되어있지만 pregnane X receptor, vitamin D receptor, constitutive androstane receptor는 주요 담즙산인 콜산(cholic acid), 데옥시콜산(deoxycholic acid), 케노데옥시콜산 대신 리토콜산(lithocholic acid) , 3-케토리토콜산(3-keto lithocholic acid) 등과 결합하는 것으로 알려져 있어 상대적으로 연구가 덜 되어 있다[4].
본고에서는 세포막에 존재하는 담즙산 수용체인 G-protein bile acid-activated receptor 1 (GPBAR1) 및 Sphingosine-1-phosphate receptor 2 (S1PR2)에 대해서 살펴보고 이들이 담도암의 병태 생리에 어떤 역할을 하는지 알아보고자 한다.
본 론FXR이 데옥시리보핵산(desoxyribonucleic acid, DNA)에 결합하는 핵수용체(neuclear receptor)인 반면에 GPBAR1과 S1PR2는 세포막에 존재하는 G 단백질 결합수용체(G protein-coupled receptor)이다(Table 1).
1. GPBAR1 (Takeda G protein-coupled receptor 5, TGR5)GPBAR1은 TGR5로 불리기도 하며 2002년 Maruyama 등[5]에 의해 발견되었다. GPBAR1은 세포내신호전달(cell signaling)을 통해 유전자 발현을 조절한다. GPBAR1의 전령리보핵산(messenger ribonucleic acid, mRNA)은 간을 포함하여 담낭, 위, 소장, 폐, 비장, 신장, 부신, 여성생식기, 지방조직, 평활근, 태반 등에 고농도로 존재하는데 특이한 점은 간내에서의 분포이다[6,7]. GPBAR1은 동모양세포(sinusoidal cell), 쿠퍼세포(Kuppfer cell), 간 내의 대식세포(liver resident macrophage) 등 간의 비실질세포에 존재하지만 간실질세포(hepatocyte)에는 발현되지 않는다[8]. 반면 후술할 S1PR2는 간에서 모든 형태의 세포에 존재한다는 점에서 GPBAR1과 차이가 있다.
GPBAR1은 대부분 자극성 G 알파 단백질(stimulatory G alpha protein, Gαs)과 작용하며 활성화된 Gαs는 아데닐산 고리화효소(adenylate cyclase) 쪽으로 이동 및 결합해서 여러 개의 cyclic adenosine monophosphate (cAMP)를 만들어 세포내로 방출한다. 하나의 cAMP는 여러 개의 다른 효소를 활성화하고 활성화된 효소는 또다른 많은 효소를 활성화하는 방식으로 세포내 신호전달이 증폭된다. 하지만 담관세포에서는 다른 세포와 달리 GPBAR1이 억제성 G 알파 단백질(inhibitory G alpha protein, Gαi)에 작용할 수 있는데, Gαs와 Gαi 중 어디에 작용하는지는 GPBAR1의 세포내 위치에 따라 달라진다. 예를들면, 담관세포의 섬모에 존재하는 GPBAR1은 Gαi에 작용하여 세포증식을 억제한다. 반면 세포막의 선단면(apical plasma membrane)에 존재하는 GPBAR1은 Gαs에 작용하여 세포증식을 촉진하는 역할을 한다[9]. GPBAR1은 protein kinase A, protein kinase B (AKT), Src kinase, Rho kinase, mammalian target of rapamycin complex 1, extracellular signal-regulated kinase 1/2 (ERK1/2) 등 다양한 kinase pathway를 활성화할 수 있다. 반대로 nuclear factor kappa-light-chain-enhancer of activated B cells (NF-ΚB) signaling은 억제하여 세포내 칼슘과 활성산소를 증가시키며 다른 이온채널의 활성화, 유전자발현 조절, 미토콘드리아 분열에 관여한다[10].
2. S1PR2S1PR2는 sphingosine-1-phosphate (S1P)에 대한 수용체이다. Sphingosine은 amino alcohol의 하나로서 세포막에 풍부한 ceramide가 ceramidase에 의해 분해되어 생성된다. S1PR은 1부터 5번까지 존재하는데 간실질세포 및 담관세포에 많이 존재하는 것은 S1PR2이다. 2012년 Studer 등[11]은 S1P 외에도 타우로콜산(taurocholic acid) 등의 결합담즙산(conjugated bile acid)이 S1PR2를 활성화할 수 있음을 보고하였다. S1PR2의 mRNA는 간, 담낭, 폐, 소장, 심장, 지방조직, 여성 생식기, 뇌, 림프절, 태반 등에서 많이 발견되는데[12,13], 간실질세포에 발현한다는 점에서 GPBAR1과 차이가 있다.
S1PR2는 리간드(ligand)와 결합하여 epidermal growth factor receptor (EGFR), insulin receptor를 활성화하며 이는 ERK, AKT (protein kinase B), c-Jun N-terminal kinase를 자극한다. 인산화된 ERK1/2는 NF-ΚB의 활성화 및 nuclear translocation을 유발하고 cyclooxygenase-2 (COX-2), interleukin-6 (IL-6), tumor necrosis factor-α 발현에 관여한다. 또한 핵 내의 sphingosine kinase 2를 상향조절(upregulation)하여 S1P의 합성을 늘리고 histone deacetylase의 기능을 억제한다. 이로써 FXR이나 small heterodimer partner (SHP), CYP7A1, apolipoprotein B-100 같은 유전자의 조절에 관여한다(Fig. 1) [14].
3. 담관세포에서 GPBAR1의 역할GPBAR1은 생쥐와 쥐, 사람 조직에서 간외담관, 간내담관, cannals of Hering의 상피세포에 존재한다. 그리고 담낭에서는 상피세포 외에 담낭 평활근에서도 발견된다[10]. 세포내에서는 섬모, 선단면, 소포체, 심지어 핵막에도 존재하며 쥐의 담즙에서 분리된 엑소좀에서도 발견되었다[9,15].
담관세포에 담즙산을 투여하면 담관세포의 증식이 관찰된다. 그리고 설치류에 담즙산을 투여하거나 총담관을 결찰해서 다량의 담즙산에 노출시키는 경우에도 비슷한 현상이 발생한다. 이처럼 담즙산이 담관세포의 증식을 유발한다는 사실은 이전부터 알려져 있었으나 그 기전이 무엇인지는 담즙산 수용체가 발견되기 이전까지 알지 못하였다[16].
GPBAR1 knockout mouse에서는 담즙산 노출 후에도 담관세포의 증식이 나타나지 않는데, 이를 통해 담즙산에 의한 담관세포 증식에 GPBAR1이 관여하리라는 것을 추정할 수 있다. 담즙산을 투여한 GPBAR1 wild type mouse에서는 ERK1/2의 인산화가 확인되는 반면 knockout mouse에서는 이를 확인할 수 없다. 따라서 GPBAR1에 의한 세포내 신호전달에 ERK1/2가 관여함을 알 수 있다. 그리고 mitogen-activated protein kinase kinase-1 (MEK-1) 억제제를 투여하는 경우에도 담즙산에 의한 wild type mouse 담관세포의 증식이 억제되는 것으로 나타나 MEK-1 역시 신호전달에 관여한다는 것을 알 수 있었다. 흥미롭게도 사이토카인이나 성장인자에 의한 담관세포증식은 GPBAR1 knockout에 영향을 받지 않는 것으로 나타나는데, 이는 GPBAR1에서 adenylate cyclase를 거치지 않고 EGFR을 거쳐서 작동하는 경로가 존재하기 때문으로 보인다[17].
GPBAR1은 담관세포의 증식 외에 담즙의 분비에도 관여한다. GPBAR1이 활성화되면 cystic fibrosis transmembrane conductance regulator (CFTR)를 통해 담관세포 밖으로 염소의 배출을 촉진한다[18,19]. 배출된 염소는 anion exchanger2 (AE2)에 의해 세포내의 중탄산염과 교환되어 세포내로 재유입되며 결과적으로 중탄산염이 풍부한 담즙이 만들어진다.
GPBAR1은 담즙산의 독성으로부터 담관세포를 보호하는 역할을 하는 것으로 보인다. GPBAR1 knockout mouse에서 유래한 담관세포는 wild type에 비해 세포자멸사(apoptosis)에 취약한데 세포사멸수용체(death receptor)에 의한 세포자멸사 경로의 변화 그리고 담관세포를 보호하는 중탄산염의 배출 저하와 관련된 것으로 생각된다[10]. GPBAR1이 담관세포의 세포자멸사에 작용하는 기전에 대해서는 뒤에서 다시 언급하고자 한다.
4. 담관세포에서 S1PR2의 역할S1PR2는 생쥐의 담관 세포주에서 발견되며 선단면 외에 담관세포 내에서 존재하는 곳은 아직 밝혀지지 않았다. S1PR2는 GPBAR1과 마찬가지로 담즙정체 시 담관세포의 증식과 관련된 것으로 나타났다. 생쥐의 담관을 결찰하면 간 및 담관세포 내의 S1PR2 mRNA가 증가되며 담즙산이나 S1P를 투여하여 S1PR2를 자극하면 ERK 및 AKT 인산화가 유발된다. 반면 S1PR2 길항제를 투여하면 ERK, AKT 인산화가 억제된다. Immortalized normal cholangiocyte에서도 비슷한 결과를 보이는데 담즙산을 투여하면 세포내 S1PR2 mRNA양이 늘어나고 세포가 증식하는 반면, S1PR2에 대한 짧은 헤어핀 리보핵산(small hairpin ribonucleic acid, shRNA)을 투여하면 세포 증식이 억제된다.
S1PR2는 담즙정체 시에 나타나는 간섬유화와도 연관된 것으로 보인다. 생쥐의 담관을 결찰하면 COX를 통한 염증반응이 발생하고 간섬유화가 진행되는데 S1PR2 knockout mouse에서는 염증 및 섬유화의 정도가 덜하다. 정리하면 담도 폐쇄 발생 시 담즙산에 의해 S1PR2가 활성화되어 담관세포가 증식하며 ERK1등을 통해 염증 반응이 유발된다. 그리고 Fig. 1에서 제시한 것처럼 S1P가 증가되면서 histone deacetylase가 억제되어 히스톤에 가려져 있던 간섬유화와 연관된 DNA에 히스톤 아세틸화가 발생한다. 히스톤이 아세틸화되면 DNA와 히스톤의 결합이 약해져서 해당 부분의 DNA는 더 많이 노출되고 이에 따라 RNA로의 전사가 촉진되는 것으로 생각된다[22].
5. 담관암에서 GPBAR1 및 S1PR2의 역할정상 담관세포와 마찬가지로 담관암세포주에 담즙산이나 GPBAR1 작용제를 투여하면 암세포의 증식이 나타난다. 이 과정에 ERK1/2와 EGFR이 관여하는 것도 정상 담관세포와 비슷하다. 아울러 암세포가 자라기 위해서는 세포자멸사를 회피해야 하는데, GPBAR1은 담관세포의 세포자멸사를 방해하는 것으로 알려졌다. 그 근거를 살펴보면, 첫째로 GPBAR1 knockout mouse에서 기원한 담관세포는 wild type에 비해 생존성이 떨어지고 세포자멸사가 증가되는 것이 확인된다. 그리고 CD 95 리간드는 세포자멸사를 촉진하는데 이러한 효과는 GPBAR1 knockout mouse에서 더 높다. GPBAR1이 활성화되면 CD95 수용체의 인산화가 촉진되며 이를 통해 세포사멸수용체가 세포내부에 머무르면서 세포자멸사를 막는 역할을 한다. 담관암 조직에서는 인산화된 CD95 수용체가 많이 발견되는 반면 정상 간조직에서는 이런 소견이 보이지 않는다[17].
S1PR2도 GPBAR1과 유사한 연구 결과를 보인다. S1PR2 길항제를 투여하거나 shRNA를 이용해서 S1PR2 expression을 억제하면 담즙산에 의한 암세포 증식이 억제되는 현상을 볼 수 있다. 담즙산은 담관암세포의 증식 외에도 invasion 및 migration을 촉진하는 것으로 알려져 있는데, 마찬가지로 S1PR2를 억제하면 invasion과 migration이 모두 억제된다[23].
생쥐의 담관암 모델에서 담즙산은 NF-ΚB의 활성도를 높여 IL-6 및 COX-2를 증가시킨다[24]. COX-2의 증가는 EGFR의 활성화를 통해 담관암세포가 성장하고 세포자멸사에 대해 저항하도록 돕는다[25]. 그리고 S1PR2에 대한 길항제는 COX-2 발현 및 EGFR 활성화를 감소시키는데, 이는 S1PR2에 대한 shRNA를 투여한 것과 유사한 결과이다[24]. 이러한 연구 결과는 S1PR2가 담즙산에 의한 COX-2 발현과 담관암의 진행에 중요한 역할을 하며 향후 담관암 치료에 중요한 표적이 될 수 있음을 시사한다[26].
결 론GPBAR1과 S1PR2는 담즙산 수용체 중에서도 대표적인 G 단백질 결합수용체이며 담관세포에 많이 존재한다. GPBAR1은 담관세포의 증식 및 분비를 유도하여 담관세포를 독성이 있는 담즙산으로부터 보호하는 역할을 한다. S1PR2도 담즙산에 의해 활성화되어 담관세포의 증식을 유발한다. 하지만 GPBAR1과 S1PR2는 정상 담관세포 외에 담관암세포에도 존재하며 암세포의 증식과 침윤을 촉진하는 것으로 밝혀졌다. 더 많은 연구를 통해 담즙산 수용체가 담관암의 진행을 유발하는 기전을 이해하고 이를 통해 담관암 환자의 진료에 획기적인 발전이 있기를 기대한다.
REFERENCES1. Makishima M, Okamoto AY, Repa JJ, et al. Identification of a nuclear receptor for bile acids. Science 1999;284:1362-1365.
2. Parks DJ, Blanchard SG, Bledsoe RK, et al. Bile acids: natural ligands for an orphan nuclear receptor. Science 1999;284:1365-1368.
3. Wang H, Chen J, Hollister K, Sowers LC, Forman BM. Endogenous bile acids are ligands for the nuclear receptor FXR/BAR. Mol Cell 1999;3:543-553.
5. Maruyama T, Miyamoto Y, Nakamura T, et al. Identification of membrane-type receptor for bile acids (M-BAR). Biochem Biophys Res Commun 2002;298:714-719.
6. Kawamata Y, Fujii R, Hosoya M, et al. A G protein-coupled receptor responsive to bile acids. J Biol Chem 2003;278:9435-9440.
7. Vassileva G, Golovko A, Markowitz L, et al. Targeted deletion of Gpbar1 protects mice from cholesterol gallstone formation. Biochem J 2006;398:423-430.
8. Keitel V, Reinehr R, Gatsios P, et al. The G-protein coupled bile salt receptor TGR5 is expressed in liver sinusoidal endothelial cells. Hepatology 2007;45:695-704.
9. Masyuk AI, Huang BQ, Radtke BN, et al. Ciliary subcellular localization of TGR5 determines the cholangiocyte functional response to bile acid signaling. Am J Physiol Gastrointest Liver Physiol 2013;304:G1013-G1024.
11. Studer E, Zhou X, Zhao R, et al. Conjugated bile acids activate the sphingosine-1-phosphate receptor 2 in primary rodent hepatocytes. Hepatology 2012;55:267-276.
12. Ishii I, Friedman B, Ye X, et al. Selective loss of sphingosine 1-phosphate signaling with no obvious phenotypic abnormality in mice lacking its G protein-coupled receptor, LP(B3)/EDG-3. J Biol Chem 2001;276:33697-33704.
13. Uhlén M, Fagerberg L, Hallström BM, et al. Proteomics. Tissue-based map of the human proteome. Science 2015;347:1260419.
14. Nagahashi M, Takabe K, Liu R, et al. Conjugated bile acid-activated S1P receptor 2 is a key regulator of sphingosine kinase 2 and hepatic gene expression. Hepatology 2015;61:1216-1226.
15. Deutschmann K, Reich M, Klindt C, et al. Bile acid receptors in the biliary tree: TGR5 in physiology and disease. Biochim Biophys Acta Mol Basis Dis 2018;1864:1319-1325.
16. Alpini G, Glaser S, Robertson W, et al. Bile acids stimulate proliferative and secretory events in large but not small cholangiocytes. Am J Physiol 1997;273:G518-G529.
17. Reich M, Deutschmann K, Sommerfeld A, et al. TGR5 is essential for bile acid-dependent cholangiocyte proliferation in vivo and in vitro. Gut 2016;65:487-501.
18. Keitel V, Cupisti K, Ullmer C, Knoefel WT, Kubitz R, Häussinger D. The membrane-bound bile acid receptor TGR5 is localized in the epithelium of human gallbladders. Hepatology 2009;50:861-870.
19. Li T, Holmstrom SR, Kir S, et al. The G protein-coupled bile acid receptor, TGR5, stimulates gallbladder filling. Mol Endocrinol 2011;25:1066-1071.
20. Lavoie B, Balemba OB, Godfrey C, et al. Hydrophobic bile salts inhibit gallbladder smooth muscle function via stimulation of GPBAR1 receptors and activation of KATP channels. J Physiol 2010;588:3295-3305.
21. Keitel V, Häussinger D. Role of TGR5 (GPBAR1) in liver disease. Semin Liver Dis 2018;38:333-339.
22. Wang Y, Aoki H, Yang J, et al. The role of sphingosine 1-phosphate receptor 2 in bile-acid-induced cholangiocyte proliferation and cholestasis-induced liver injury in mice. Hepatology 2017;65:2005-2018.
23. Liu R, Zhao R, Zhou X, et al. Conjugated bile acids promote cholangiocarcinoma cell invasive growth through activation of sphingosine 1-phosphate receptor 2. Hepatology 2014;60:908-918.
24. Liu R, Li X, Qiang X, et al. Taurocholate induces cyclooxygenase-2 expression via the sphingosine 1-phosphate receptor 2 in a human cholangiocarcinoma cell line. J Biol Chem 2015;290:30988-31002.
Fig. 1.Model of S1PR2 action. S1PR2, Sphingosine-1-phosphate receptor 2; ERK1/2, extracellular signal-regulated kinase 1/2; SphK2, Sphingosine kinase 2; S1P, sphingosine-1-phosphate; HDAC, histone deacetylase; NF-ΚB, nuclear factor kappa-light-chain-enhancer of activated B cells. 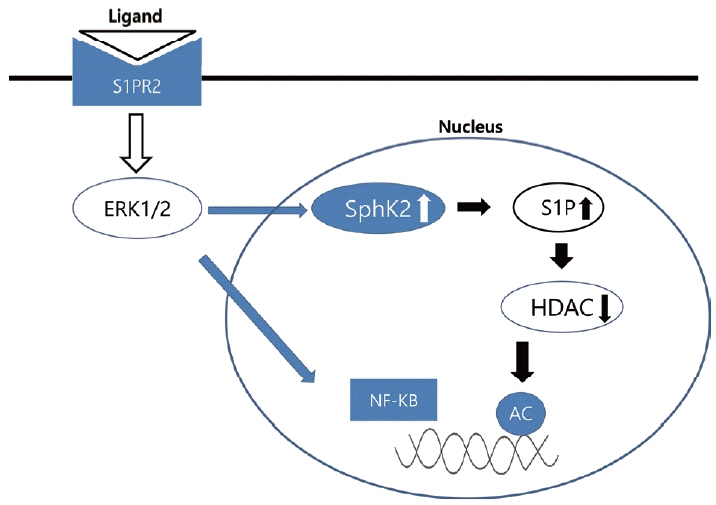
Table 1.The classification of bile acid receptors (modified from Fiorucci and Distrutti [10]) FXR, farnesoid X receptor; CDCA, chenodeoxycholic acid; CA, cholic acid; LCA, lithocholic acid; DCA, deoxycholic acid; VDR, vitamin D receptor; PXR, pregnane X receptor; CAR, constitutive androstane receptor; GPBAR1, G-protein bile acid-activated receptor 1; UDCA, ursodeoxycholic acid; S1PR2, sphingosine-1-phosphate receptor 2; GCA, glycocholic cid; TCA, taurocholic acid; GCDCA, glyco chenodeoxycholic acid; TCDCA, taurochenodeoxycholic acid; GDCA, glycodeoxycholic acid; TDCA, taurodeoxycholic acid. |
|
|||||||||||||||||||||||||||||||||||||
|
|||||











