서 론
급성 췌장염은 담석, 음주, 약물, 복부 외상, 고중성지방혈증 및 고칼슘혈증과 같은 대사장애, 감염 등의 다양한 원인에 의해 췌장선 세포의 손상이 발생하고 광범위한 간질성 부종이 발생하는 췌장의 염증성 질환이다. 급성 췌장염의 80%에서는 경한 임상양상을 보이고 보존적인 치료로 대부분 호전되지만, 20%는 괴사성 췌장염으로 진행하게 된다. 괴사성 췌장염은 사망률이 15%에 이르고 20-35%에서 감염이 동반될 수 있으며 감염이 동반될 경우 패혈증과 다발성 장기 부전이 발생하여 사망률이 더욱 증가하게 된다[1]. 따라서 임상 양상과 진단 검사 및 영상 검사를 통한 정확한 진단과 적절한 치료가 필요하다. 고전적으로 괴사성 췌장염의 치료로 수술적 괴사 제거술이 많이 시행되었으나 최근에는 경피적 배액술과 내시경적 괴사 제거술을 포함한 최소침습적 시술이 괴사성 췌장염 치료에 널리 이용되고 있다. 경피적 배액술과 내시경적 괴사 제거술과 같은 치료법은 기존의 수술적 괴사 제거술과 비교하여 덜 침습적이고 더욱 안전하며 효율적으로 괴사성 췌장염을 치료할 수 있다[2]. 저자들은 괴사성 췌장염 환자에서 완전 피복 식도 금속 스텐트(fully covered esophageal metal stent)를 이용하여 경피적 내시경적 괴사 제거술로 대장 주변(paracolic gutter)으로 연장된 막으로 둘러싸인 괴사(walled-off necrosis)를 성공적으로 치료한 사례들을 경험하였기에 문헌 고찰과 함께 보고하는 바이다.
증 례
증례 1
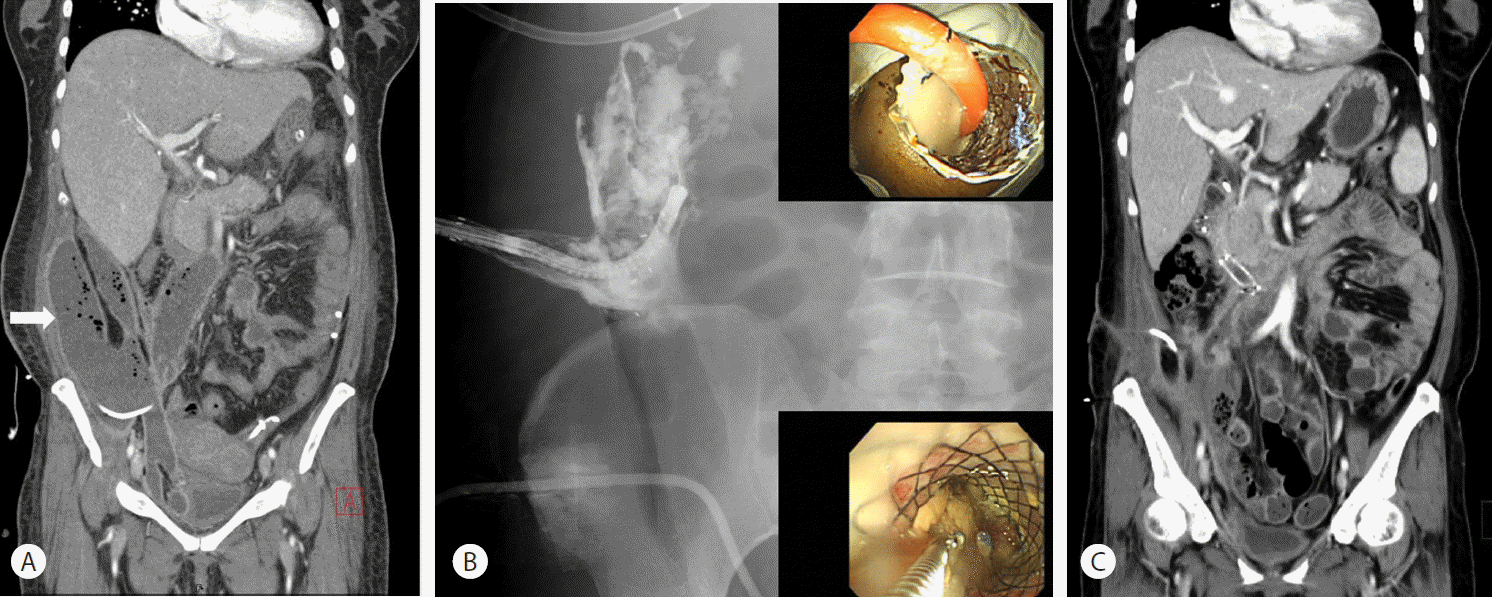
52세 여자 환자가 복통과 황달을 주소로 응급실에 내원하였다. 환자는 내원 6개월 전 운전자 교통사고로 복부 둔상을 입었고 당시 시행한 복부 전산화 단층촬영(computerized tomography)과 내시경 역행 담췌관 조영술(endoscopic retrograde cholangiopancreatography) 결과 American Association for the Surgery of Trauma에서 제시하는 췌장 외상 분류에 따라 췌장의 타박상이 있으나 췌관 손상이 없는 췌장 손상 grade II 소견을 보였다. 환자는 응급실 내원 전 췌장 외상에 의한 괴사성 췌장염으로 4개의 경피적 배액관을 가지고 있었다. 응급실 내원 당시 급성 병색을 보였으며 말초 혈액 검사에서 백혈구 13,400/mm3, 혈색소 7.3 g/dL, 혈소판 83,000/mm3, amylase 28 U/L, lipase 56 U/L, aspartate aminotransferase 26 IU/L, alanine aminotransferase 11 IU/L, alkaline phosphatase 168 IU/L로 확인되었고 total bilirubin 5.8 mg/dL, direct bilirubin 4.2 mg/dL, C-reactive protein이 21.84 mg/dL로 증가되었다. 내시경 초음파 검사(endoscopic ultrasound)에서 췌장의 몸통에 막으로 둘러싸인 췌장 괴사(walled-off pancreas necrosis)가 관찰되었고 복부 전산화 단층촬영에서 막으로 둘러싸인 괴사가 우측 대장 주변(paracolic gutter)으로 연장되어 있는 소견을 보였다(Fig. 1A). 경피적 배액관을 통하여 배액된 액체를 배양한 결과 carbapenem-resistant Acinetobacter baumannii, carbapenem-resistant Enterobacteriaceae, methicillin-resistant Staphylococcus aureus가 동정되었고 항균제 감수성 결과에 따라 적절한 항생제를 투여하였다. 경피적 배액술 및 적절한 항생제 사용에도 불구하고 임상 경과 호전 보이지 않아 입원 15일째 경피적 배액관 도관 삽입 자리에 형성된 누공을 통하여 완전 피복 식도 금속 스텐트(직경 18 mm, 길이 12 cm; Taewoong Medical, Seoul, South Korea)를 삽입하였다. 이후 CRE 풍선(Boston Scientific, Natick, Mass)을 사용하여 식도 금속 스텐트가 충분히 확장될 수 있도록 하였고 직경 5.5 mm의 비강 내시경(GIF-XP260N, Olympus)을 사용하여 경피적 내시경적 괴사 제거술을 시행하였다(Fig. 1B). 2일 간격으로 총 3차례의 경피적 내시경적 괴사 제거술로 다량의 조직 파편(necrotic debris)을 제거하였고 3번째 괴사 제거술에서 조직 파편의 현격한 감소를 확인한 후 식도 금속 스텐트를 제거하였다. 3차례의 시술 후 검사한 복부 전산화 단층촬영에서 췌장 주위에서 대장 주변까지 연장된 막으로 둘러싸인 괴사는 현저하게 감소되었다(Fig. 1C). 이후 발열과 복통이 호전되었고 검사실 소견상 C-reactive protein이 감소하고 total bilirubin이 정상화되어 퇴원하였다.
증례 2
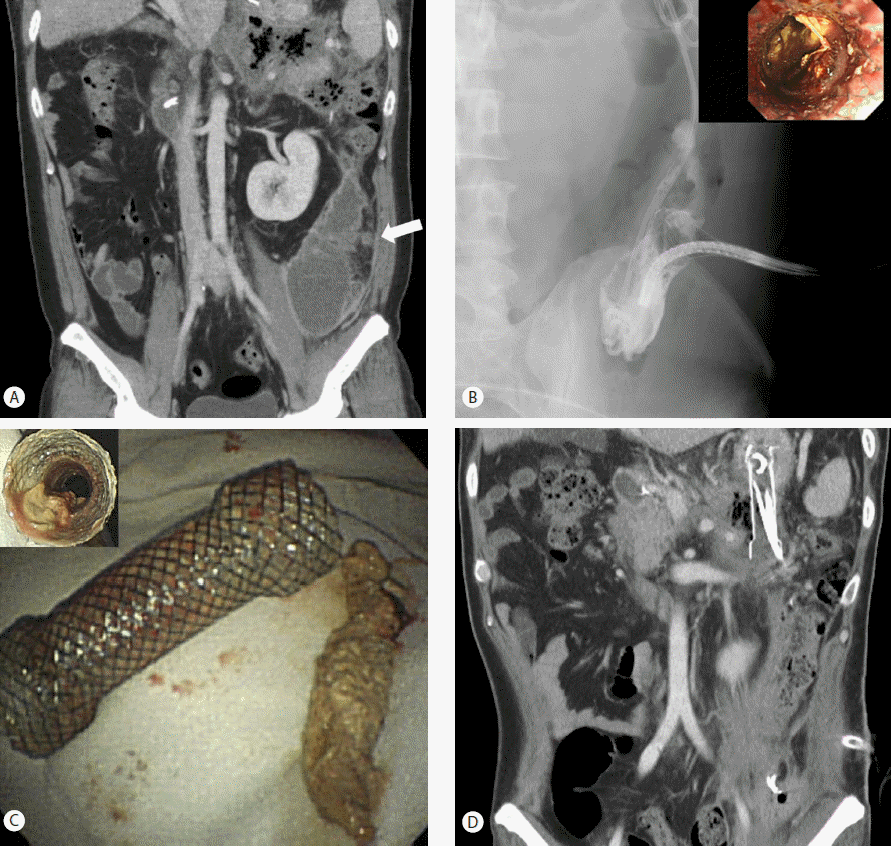
39세 남자 환자가 심와부 통증을 주소로 내원하였다. 평소 음주를 자주 하던 분으로 내원 당시 체온이 38.3°C로 확인되었고 황달을 보였다. 말초 혈액 검사에서 백혈구 증가증 및 C-reactive protein 상승이 확인되었고 혈청 amylase와 lipase가 정상 범위의 10배 이상 상승되어 있었다. 복부 전산화 단층촬영에서 췌장의 부종과 췌장 주위의 액체 고임, 담낭의 부종이 관찰되었고 담석 췌장염으로 판단하여 내시경 역행 담췌관 조영술을 시행하였다. 내시경 역행 담췌관 조영술을 통하여 담즙 슬러지를 제거하였고 2개의 플라스틱 스텐트를 삽입하였다. 이후 통증 조절, 항생제 투약을 포함한 보존적 치료 후 임상 경과 호전되어 퇴원하였다. 퇴원 2주 후 복통으로 다시 입원하였고 복부 전산화 단층촬영에서 췌장 꼬리와 왼쪽 후복막 공간에 막으로 둘러싸인 괴사가 관찰되었다(Fig. 2A).
내시경 초음파에서 췌장 꼬리에 6 cm 크기의 막으로 둘러싸인 췌장 괴사가 관찰되었고 배액을 원활하게 하기 위해 2개의 스텐트를 삽입하여 경벽적 배액술(transmural drainage)을 시행하였다. 5일 후 39°C의 발열이 발생하여 추적한 복부 전산화 단층촬영에서 이전보다는 감소되었으나 여전히 췌장 꼬리와 왼쪽 후복막 공간에 공기를 포함한 액체 고임이 관찰되었고 완전 피복 금속 스텐트를 삽입하여 내시경적 배액술(endoscopic transluminal drainage)을 시행하였으며 두 개의 이중 돼지꼬리형 요도 카테터를 좌측 신장 주변 공간에 삽입하였다. 이후 임상 경과가 호전되어 퇴원하였다. 두 번째 퇴원한 지 2주 후 발열로 재입원하였고 복부 전산화단층촬영에서 이전보다는 감소하였으나 여전히 막으로 둘러싸인 괴사가 관찰되었고 경피적 배액술과 4회의 내시경적 괴사 제거술을 시행하였으나 임상 경과 호전 없어 경피적 배액관을 제거하고 완전 피복 식도 금속 스텐트(직경 20 mm, 길이 6 cm; Taewoong Medical, Seoul, South Korea)를 왼쪽 대장 주변부(paracolic gutter)에 삽입하였다. 이후 CRE 풍선(Boston Scientific, Natick, Mass)을 사용하여 식도 금속 스텐트가 충분히 확장될 수 있도록 하였고 직경 5.5 mm의 비강 내시경(GIF-XP260N, Olympus)을 사용하여 경피적 내시경적 괴사 제거술을 시행하였으며 다량의 조직파편이 제거되었다(Fig. 2B). 2일 후 두 번째 경피적 내시경적 괴사 제거술이 시행되었고 시술 후 조직 파편이 현저하게 감소한 것을 확인하였으며 식도 금속 스텐트는 시술 종료와 함께 제거되었다(Fig. 2C). 7일 후 추적한 복부 전산화 단층촬영 결과 왼쪽 대장 주변부(paracolic gutter)와 췌장 주변의 막으로 둘러싸인 괴사는 현저하게 감소하였다(Fig. 2D).
고 찰
급성 췌장염 환자의 80%는 경한 임상양상을 보이고 통증 조절, 수액 및 영양 공급, 췌장염 유발 요인에 대한 치료를 시행할 경우 수일 내 호전된다. 그러나 20%의 환자에서는 췌장의 괴사가 발생하게 되고 이는 높은 이환율 및 사망률과 연관되어 있는 것으로 알려져 있다[1]. 괴사성 췌장염은 췌장 실질의 괴사가 동반되는 염증성 질환으로 새로 개정된 2012 급성 췌장염 Atlanta 분류에 따르면 괴사성 췌장염은 질환의 발병 시점에 따라 발병한 지 4주 이내이고 분명한 막이 없는 급성 괴사성 고임(acute necrotic collection)과 발병한 지 4주 이후이고 분명한 막이 형성된 막으로 둘러싸인 괴사로 나뉘어 진다[3]. 괴사성 췌장염 환자에서 보존적 치료를 하면서 내시경 시술 또는 수술적 치료는 정상 췌장 조직과 괴사된 췌장 조직 사이의 경계가 명확해지는 췌장염 발생 4-6주 후에 시행하는 것이 권고되고 있고 이는 시술 중 출혈과 같은 합병증을 감소시키고 불필요한 정상 췌장 조직의 절제를 감소시키는 것과 연관되어 있다[4]. 괴사성 췌장염 환자의 주된 사망 원인은 췌장 감염과 동반된 패혈증과 다발성 장기 부전이다[5]. 감염은 췌장 실질 괴사와 인접한 부위에 있는 위장관계로부터 세균의 전파에 의해서 발생하는 것으로 알려져 있고 감염을 일으키는 흔한 균에는 Escherichia coli, Staphylococcus aureus, Enterococcus faecalis 등이 있다[6]. 감염은 질병의 기간 중 어느 때나 발생할 수 있으나 보통 질병이 발생한 지 2-4주 사이에 가장 흔하게 발생하고 일반적인 항생제 치료에도 불구하고 임상적으로 악화를 보이는 경우 내시경 초음파 유도하에 췌장 및 췌장 주위 액체 고임을 세침 흡인하여 그람 염색 및 세균 배양으로 췌장 감염을 진단할 수 있다[7]. 감염성 괴사의 경우 즉시 항생제를 투여하고 감염 부위의 배액이나 내시경 및 수술적 치료와 같은 중재적 시술이 필요하다. 수술적 괴사 제거술은 전통적으로 중증의 급성 췌장염 환자에서 치료의 표준으로 여겨졌다. 하지만 수술적 괴사 제거술은 수술에 따르는 사망률이 높고 입원 기간이 길며, 수술 부위 감염, 탈장, 출혈, 장누공 등의 합병증이 발생할 수 있을 뿐만 아니라 전신 염증 반응 증후군(systemic inflammatory response syndrome)을 악화시켜 다발성 장기 부전에 이르는 경우가 종종 발생하게 된다[8]. 현재 괴사성 췌장염은 경피적 배액술, 내시경적 괴사 제거술 또는 비디오 후복막강 변연 절제술(video-assisted retroperitoneal debridement)과 같은 최소 침습 시술을 이용하여 치료하는 것이 보편적으로 받아들여지고 있고[2,9] 막으로 둘러싸인 괴사와 췌장 주위 액체 고임(peripancreatic fluid collection)을 치료하는 다양한 방법들이 소개되고 있다. 내시경적 배액술을 사용한 예로, Attam 등[10]은 10 cm 이상 크기의 막으로 둘러싸인 괴사가 있는 10명의 환자에서 대구경 완전 피복 식도 금속 스텐트(large bore, fully covered esophageal stent)를 사용하여 내시경적 배액술(endoscopic transluminal drainage)을 시행하여 막으로 둘러싸인 괴사를 치료한 사례를 보고하였다. 또한 Varadarajulu 등[11]은 막으로 둘러싸인 췌장 괴사와 위장관계 사이에 내시경 초음파를 통해 2-3개의 경벽관(transmural tract)을 생성하여 다수의 스텐트를 사용한 경벽적 배액술(transmural drainage)과 하나의 경벽관을 통한 경벽적 배액술로 췌장 괴사를 치료한 사례를 비교한 연구 결과를 보고하였다. 막으로 둘러싸인 췌장 괴사가 있는 60명의 환자 중 12명에서 2-3개의 다수의 경벽관을 통하여 내시경적 배액이 시행되었고 48명에서 하나의 경벽관을 통하여 내시경적 배액이 시행되었으며 다수의 경벽관을 통한 내시경적 배액술의 경우 91.7%의 치료 성공률을 나타내었고 하나의 경벽관을 통한 내시경적 배액술은 52.1%의 치료 성공률을 보여주어 다수의 경벽관을 통한 내시경적 배액술의 유용성에 대해 보고하였다[11]. 하지만 골반강이나 대장 주변과 같이 내시경이 접근하기 어려운 위치에 액체 고임이나 막으로 둘러싸인 괴사가 있을 경우 내시경적 배액술만으로 임상 경과의 호전을 기대하기는 어렵다. 경피적 배액술은 내시경이 접근하기 어려운 위치에 액체 고임이 위치해 있거나 액체 고임의 막이 덜 성숙되어 있을 때 유용하게 사용될 수 있으며, 최근에는 경피적 배액술과 내시경적 괴사 제거술의 유용성을 접목하여 경피적 내시경적 괴사 제거술을 시행하여 감염성 췌장 괴사를 치료한 사례가 여러 기관에서 보고되고 있다. Dhingra 등[12]이 165명의 환자를 대상으로 수행한 연구에 따르면, 103명의 괴사성 췌장염 환자들 중 74명에서 감염성 췌장 괴사가 발생하였고 이 중 15명에서 경피적 내시경적 괴사 제거술이 시행되었다. Dhingra 등[12]은 감염성 췌장 괴사가 있는 복강에 16F-18F의 튜브를 경피적으로 삽입하였고 2-3일 후 CRE 풍선을 사용하여 관(tract)을 확장한 이후 튜브를 통한 내시경적 괴사 제거술을 시행하였다. 평균 5회의 시술이 시행되었고 14명의 환자가 추가적인 시술 없이 퇴원하였다. Kedia 등[13]은 완전 피복 식도 금속 스텐트를 사용하여 경피적 내시경적 괴사 제거술로 후복막강에 위치한 액체 고임을 치료한 사례를 보고하였고 국내에서도 배액관 도관 삽관 자리를 통한 경피적 내시경적 괴사 제거술을 시행한 1예가 보고된 바가 있으나[14] 현재까지 본 증례와 같이 완전 피복 식도 금속 스텐트를 사용하여 경피적 내시경적 괴사 제거술을 시행한 예는 국내에서 보고된 바가 없다.
식도 금속 스텐트는 일반적으로 식도암으로 인한 식도 협착에 주로 사용하고 스텐트의 팽창력이 크며 유연성이 우수하다. 본 증례에서는 식도 금속 스텐트의 팽창력과 유연성을 이용하였고 식도 금속 스텐트를 사용할 경우 기존의 경피적 배액술에 사용하는 카테터나 담도 스텐트와 비교할 때 직경이 더 크기 때문에 다량의 조직파편이 쉽고 빠르게 제거될 수 있어 피부로 삽입된 스텐트를 조기에 제거할 수 있다. 증례 1의 환자에서는 2일 간격으로 총 3회의 경피적 내시경적 괴사 제거술을 시행한 후 식도 금속 스텐트를 제거하였고 증례 2의 환자에서는 2일 간격으로 총 2회의 경피적 내시경적 괴사 제거술을 시행한 후 식도 금속 스텐트를 제거할 수 있었다. 결과적으로 증례 1의 환자는 6일, 증례 2의 환자는 2일 동안 식도 금속 스텐트를 유지하였고 스텐트를 경피적으로 삽입 및 제거하는 과정에서 기술적으로 어려운 점은 없었다. 또한 내시경이 식도 금속 스텐트를 쉽게 통과할 수 있어 내시경 의사가 용이하게 내시경적 괴사 제거술을 시행할 수 있다. 기존의 연구에서 사용한 16F-18F의 튜브를 사용할 경우 수일 간격으로 CRE 풍선을 사용한 관의 단계적 확장이 필요하나 식도 금속 스텐트를 사용할 경우 CRE 풍선을 사용한 스텐트 팽창이 쉽게 이루어져 삽입과 동시에 내시경적 괴사 제거술을 시행할 수 있고 다량의 조직파편 제거를 통하여 괴사 제거술의 시행 횟수와 시술 시간이 감소하게 된다.
결론적으로 완전 피복 식도 금속 스텐트를 사용한 경피적 내시경적 괴사 제거술은 기존의 내시경적 괴사 제거술이나 경피적 배액술보다 내시경 시행 횟수와 시술 시간이 감소하고 더욱 효율적이고 빠르게 막으로 둘러싸인 괴사를 치료할 수 있다. 첫 번째 증례에서는 우측 복강에 식도 금속 스텐트를 삽입하여 우측 대장 주변으로 연장된 막으로 둘러싸인 괴사를 경피적 내시경적 괴사 제거술로 치료하였고 두 번째 증례에서는 좌측 복강에 식도 금속 스텐트를 삽입하여 막으로 둘러싸인 괴사를 치료하였으며 시술 후 출혈, 누공, 탈장 등의 합병증이 발생하지 않았다. 본 증례는 기존의 경피적 또는 내시경적 배액술을 일차적으로 시행하였음에도 불구하고 임상적인 호전을 보이지 않는 괴사성 췌장염 환자에서 직경이 큰 완전 피복 식도 금속 스텐트를 사용하여 경피적 내시경적 괴사 제거술로 대장 주변으로 연장된 막으로 둘러싸인 괴사를 치료한 예로 내시경이 접근하기 어려운 위치에 액체 고임이나 막으로 둘러싸인 괴사가 있는 괴사성 췌장염 환자에게서 효율적인 치료 방법의 하나로 사용될 수 있을 것이다. 기존에 사용하던 플라스틱 튜브와 비교하여 직경이 큰 완전 피복 금속 스텐트(fully covered metal stent)가 팽창성 및 유연성을 고려할 때 경피적 내시경적 괴사 제거술에 유용하게 사용될 수 있고 앞으로 금속 스텐트를 사용한 경피적 내시경적 괴사 제거술에 대한 다기관 연구를 통하여 시술 적응증과 치료 성공률, 주요 합병증에 대한 추가적인 연구가 필요하다.