서 론
선형 내시경 초음파(endoscopic ultrasound, EUS)의 발달로 내시경 초음파를 이용한 여러 중재적 시술이 가능해졌다. 췌담도 영역에서 내시경 초음파 유도하 배액술(EUS-guided drainage)은 기존의 침습적 치료를 대체할 수 있을 것으로 기대되며 점차 널리 사용되면서 적응증을 넓혀가고 있다. 하지만 아직까지 내시경 초음파 유도하 배액술에 특화된 부속 기구들이 부족하여 주로 내시경역행담췌관조영술(endoscopic retrograde cholangiopancreatography, ERCP)에 사용되는 부속 기구들이 주로 사용되고 있다. 내시경 초음파 유도하 배액술은 ERCP와는 달리 복강을 통과하여 위나 장과 담관, 담낭, 췌관 혹은 가성 낭종을 연결하는 시술이기 때문에 합병증의 발생 위험성이 있어 이를 예방할 수 있는 전용 기구와 스텐트의 개발이 꼭 필요하다. 최근에는 이러한 내시경 초음파 유도하 배액술에 특화된 다양한 스텐트들이 개발되면서 좀 더 효과적이고 안전한 시술이 가능해지고 있다. 이번 고찰에서는 각종 내시경 초음파 유도하 배액술을 위해 개발된 스텐트들의 종류와 특징들을 살펴보고, 이러한 스텐트를 활용한 배액술의 임상 성적에 대해 살펴보도록 하겠다.
본 론
1. 새롭게 개발된 스텐트
1) Lumen-apposing metal stents (LAMS)
최근 개발된 LAMS는 초음파 내시경 유도하 경벽 배액술을 위해 개발된 스텐트로서 두 구조물(non-adherent structures)을 밀착시켜서 스텐트 이탈(stent migration)이나 누출(leakage)을 최소화할 수 있도록 고안된 스텐트를 일컫는다(Fig. 1). 스텐트 플랜지(flange)가 크고 길이가 짧은 특유의 아령 모양 형태로 되어 있고, 전통적으로 사용되던 금속 스텐트보다 직경이 커서 효과적인 배액이 가능하고 위장관 벽 외 구조물(extraluminal structure)에 대한 접근이 용이하다. AXIOS™ (Boston Scientific, Natick, MA, USA)는 최초로 개발된 LAMS로서 니티놀 금속사와 실리콘 피막으로 구성되며, 바벨 모양의 형태로 두 구조물을 밀착시켜 주어서 스텐트 이탈이나 누출의 위험성을 낮출 수 있도록 고안되었다[1]. 스텐트 직경은 6, 8, 10, 15, 20 mm가 있고, 플랜지 사이의 길이(saddle length)는 10 mm이며 전달용 카테터는 10.8 Fr이다. 최근에는스텐트전달시스템의선단(tip)에 전기소작 기능을 탑재한 electrocautery-enhanced LAMS (EC-LAMS)인 Hot AXIOS™가 개발되어 누공 확장을 위한 기구 교환(accessory exchange) 등의 복잡한 절차 없이 단일 과정(single step)으로 스텐트 전달을 가능하게 하여 시술을 용이하게 하고 합병증의 위험을 낮출 수 있을 것으로 기대된다. 또 다른 LAMS인 Niti-S SPAXUS™ (Taewoong Medical Co., Ltd., Ilsan, Korea)는 니티놀 금속사와 실리콘 피막으로 구성되며 양쪽 끝에 스텐트 고정을 위한 큰 플랜지가 있고, margin은 둥글게 하여 낭종 벽에 외상을 최소화할 수 있도록 하였다[2]. 직경은 8, 10, 16 mm가 있고, 스텐트 길이(플랜지 사이 거리)는 20 mm이다. 스텐트 전개 과정에서 플랜지가 젖혀지면서 7 mm까지 감소하도록 설계되어 두 벽을 밀착시킨다. 10 Fr의 전통적인 스텐트 전달 시스템(conventional delivery system)을 사용하여 recapture가 가능하다는 장점이 있다. 최근에는 전기 소작 기능을 탑재한 EC-LAMS인 Niti-S HOT SPAXUS™가 개발되었다[3].
2) Modified tubular metal stents
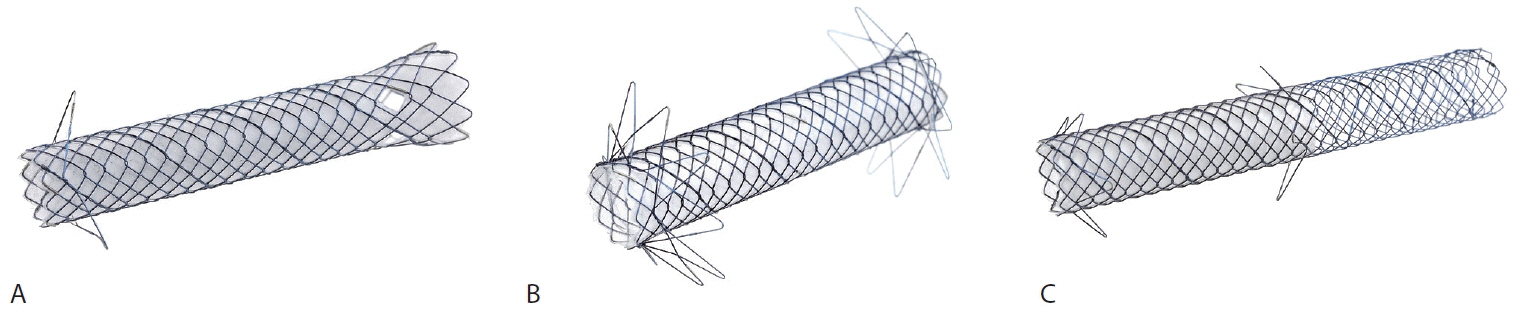
LAMS 외에도 내시경 초음파 유도하 경벽 배액술을 위해 이탈 방지 기능을 갖는 다양한 완전 피막형 또는 부분 피막형의 금속 스텐트가 개발되었다. NAGI 스텐트(Taewoong Medical Co., Ltd.)는 스텐트 이탈 방지를 위해 양쪽 선단에 넓은 flare (직경 20 mm)가 있으며, 다양한 스텐트 직경(10, 12, 14, 16 mm)과 길이(10, 20, 30 mm)가 가능하다[4]. 스텐트 전달 시스템은 9 Fr 또는 10 Fr이며, 스텐트 원위부 플랜지에 끈(suture)이 부착되어 스텐트 제거를 용이하게 할 수 있도록 하였다. BONA-SOO 스텐트(Standard Sci Tech Inc., Seoul, Korea) (Fig. 2A)는 가성 낭종 배액술을 위해 고안된 스텐트로 니티놀 금속사와 실리콘 피막으로 구성되며, 근위부 이탈(proximal migration)을 방지하기 위해 근위부에 flap이 있고, 원위부에는 sidehole이 있어 가성 낭종이 배액되면서 수축하는 과정에서도 배액이 용이하게 이루어질 수 있도록 하였다[5]. 스텐트 직경은 8-10 mm, 길이는 3-5 cm가 있으며 전달용 카테터의 직경은 8.5 Fr이다. BONA-AL 스텐트(Standard Sci Tech Inc., Seoul, Korea) (Fig. 2B)는 경벽 배액술을 위해 개발된 스텐트로 니티놀 금속사와 실리콘 피막으로 구성되며, 스텐트 전개 후에 양쪽 선단이 90도의 angulation (외경 22 mm)을 갖도록 설계되어 스텐트 이탈을 방지할 수 있도록 하였다. 스텐트 직경은 10 mm이며 길이는 4-7 cm이다[6]. Hybrid metal stent (Standard Sci Tech Inc., Seoul, Korea) (Fig. 2C)는 담도배액술을 위해 고안된 부분 피막형 금속 스텐트로서 스텐트 원위부 3.5 cm는 실리콘 피막의 니티놀 금속사로 되어 있어 담즙 누출을 방지할 수 있도록 하였고, 피막 부분에 근위부 이탈과 원위부 이탈을 방지하기 위한 2개의 flap이 있다[7]. 스텐트 직경은 8-10 mm, 길이는 5-9 cm이다. Giobor 스텐트(Taewoong Medical Co., Ltd.)는 간위연결술을 위해 고안된 부분 피막형 금속 스텐트로 스텐트의 근위부 1 cm 부분은 피막이 없고, 원위부는 flared portion으로 되어 있어 스텐트 이탈을 방지할 수 있도록 하였다[8]. 스텐트 직경은 8, 10 mm이고, 길이는 8, 10, 12 cm이다. 그 밖에도 간위연결술 용도로 개발된 Spring Stopper (Taewoong Medical Co., Ltd.), 5.9 Fr의 얇은 스텐트 전달 시스템을 갖는 HANAROSTENT Biliary Full cover Benefit (M.I Tech, Seoul, Korea) 등이 개발되어 연구되고 있다[9,10].
3) 플라스틱 스텐트
Through & Pass IT type stent (Gadelius Medical Co., Ltd., Tokyo, Japan)는 간위연결술을 위해 개발된 플라스틱 스텐트이다[11]. Push-type 스텐트로서 스텐트 길이는 20 cm, 유효 길이는 15 cm이다. 스텐트 근위부 선단은 돼지꼬리 모양으로 되어 있고, 원위부 선단은 점차 가늘어지는(tapered) 모양으로 되어 있으며, 스텐트 이탈 방지를 위해 4개의 플랜지(원위부 2개, 근위부 2개)가 있다.
2. 내시경 초음파 유도하 배액술의 성적
1) 가성 낭종 배액술(EUS-guided pseudocyst drainage)
가성 낭종의 경벽 배액술에 있어서 전통적으로는 이중 돼지꼬리형 플라스틱 스텐트(double pigtail plastic stent)가 주로 사용되었으나, 최근에는 보다 넓은 직경으로 효과적인 배액을 가능하게 하고, 스텐트 폐쇄의 위험을 낮출 수 있는 금속 스텐트가 많이 사용되고 있다. Itoi 등[12]은 15명의 증상을 동반한 가성 낭종(symptomatic pseudocyst) 환자에서 AXIOS stent를 이용한 경벽 배액술을 시행하여 100%의 기술적 성공률과 임상적 성공률을 확인하였다. 스텐트 이탈이 1건에서 있었으며, 11.4개월 동안 가성 낭종의 재발은 없었다. 최근 전향 연구에서 61명의 췌장주위액체고임(peripancreatic fluid collection) 환자(구역성 췌장괴사 46명, 가성 낭종 15명)에서 AXIOS를 이용한 경벽 배액술의 기술적 성공률은 98%, 임상적 성공률은 93%였으며 중대한 합병증은 천공 1건이 있었다[13]. SPAXUS를 이용한 경벽 배액술은 최초 보고에서 1명의 구역성 췌장괴사와 3명의 가성 낭종 환자에서 100%의 성공률을 보고하였고, 합병증은 없었다[2]. 국내 다기관 전향 연구에서 34명의 증상을 동반한 췌장 가성 낭종 환자를 대상으로 SPAXUS를 이용한 경벽 배액술의 기술적 성공률은 97.1%, 임상적 성공률은 94.1%였다[14]. 시술 관련 또는 스텐트 관련 이상반응은 4명(11.8%)에서 발생하였는데, maldeployment 1건, 가성 낭종 감염 3건이었다. 가성 낭종에서 LAMS와 플라스틱 스텐트를 직접적으로 비교한 연구는 많지 않다. Bang 등[15]의 후향 연구에 따르면 LAMS와 플라스틱 스텐트는 기술적 성공률(100% vs. 100%)과 치료 성공률(100.0% vs. 92.9%), 이상반응(0.0% vs 21.4%)에 있어 통계적으로 유의한 차이가 없었다.
2) 구역성 췌장괴사 배액술(EUS-guided walled-off necrosis drainage)
구역성 췌장괴사 배액술에서 LAMS는 직경이 넓어 효과적인 배액이 가능하고 내시경적 괴사 제거술(direct endoscopic necrosectomy)이 용이하다는 장점이 있다. 최근 체계적 문헌고찰과 메타분석에 따르면 구역성 췌장괴사 배액술에 있어 금속 스텐트는 플라스틱 스텐트에 비해서 overall resolution rate가 높았고(92.1% vs. 80.9%; OR 2.8; p=0.001), 출혈의 위험성, 스텐트 폐쇄와 천공의 위험성은 더 낮은 경향성을 보였으나 통계적으로 유의한 차이는 없었다[16]. LAMS와 플라스틱 스텐트를 비교하였을 때에는 LAMS가 플라스틱 스텐트에 비해서 overall resolution rate가 더 높았지만(91.5% vs. 80.9%; OR 2.5; p=0.001), 한 번의 내시경 시술 후 resolution rate는 두 스텐트 간에 통계적으로 유의한 차이가 없었다(52.3% vs. 43.4%, p=0.4). 그러나, 최근 Bang 등[17]의 무작위 배정 임상 시험에서는 구역성 췌장괴사 배액술에서 LAMS와 플라스틱을 비교하였을 때, 총 시술 횟수와 치료 성공률, 이상반응, 재입원, 입원 기간 등에 있어서 두 군 사이에 통계적으로 유의한 차이가 없었다. LAMS는 플라스틱 스텐트에 비해 시술 시간이 통계적으로 유의하게 짧았으나, 스텐트와 관련된 이상반응(32.3% vs. 6.9%, p=0.01)과 비용(US$12,155 vs. US$6,609, p<0.001)은 LAMS군에서 더 높았다. LAMS와 관련된 이상반응에 대한 우려도 있다. 한 전향 연구에서는 LAMS군의 절반 정도에서 출혈, buried LAMS syndrome, 담도 폐쇄 등 후기 상반응(delayed adverse event)이 발생하였다[18]. 췌장액체고임에서 LAMS를 이용한 경벽 배액술 시행 시 출혈 위험이 높고 내시경적 재시술의 필요성이 높다는 보고들도 있다[19,20]. 유럽 소화기내시경학회(European Society of Gastrointestinal Endoscopy)에서는 스텐트 관련 이상반응을 방지하기 위해 LAMS를 삽입한 경우 4주 이내에 제거할 것을 권고하고 있다[21].
3) 내시경 초음파 유도하 담낭 배액술(EUS-guided gallbladder drainage, EUS-GBD)
EUS-GBD에서는 피막형 자가 팽창형 금속 스텐트와 LAMS가 주로 사용된다. 변형된 피막형 금속 스텐트인 BONA-AL stent를 이용한 EUS-GBD의 초기 연구 결과에서 15명을 대상으로 실행 가능성과 안전성을 확인하였다[6]. 이후 56명의 환자를 대상으로 한 장기 추적 관찰 보고(중앙 추적 관찰 기간 275일)에서 54명의 환자(96.4%)가 급성 담낭염의 재발이 없었다. 후기 이상반응은 4명 (7.1%)에서 발생하였으며, 무증상의 원위부 스텐트 이탈 2건, 스텐트 폐쇄로 인한 급성 담낭염 2건이 있었다. 같은 기관에서 BONA-AL stent와 SPAXUS를 이용한 EUS-GBD를 비교하였을 때 기술적 성공률(100% vs. 94%; p=0.49), 임상적 성공률(100% vs. 94%; p=0.49), 시술 관련 이상반응(2.9% vs. 0.0%; p=0.99), 스텐트 관련 후기 이상반응(5.8% vs. 11.8%; p=0.43), 6개월 담낭염 재발률(3.1% vs. 3.4%; p=0.99), 1년 재발률(3.1% vs. 8.3%; p=0.56)에 있어 통계적으로 유의한 차이가 없었다[22].
LAMS는 담낭과 장벽(또는 위벽)을 밀착시켜줌으로써 담즙 누출과 스텐트 이탈을 방지할 수 있고, 직경이 커서 배액을 효과적으로 할 수 있는 장점이 있다. AXIOS를 이용한 EUS-GBD의 초기 연구에서 시술을 시행한 5명의 급성 담낭염 환자에서 시술 관련 합병증 없이 급성 담낭염이 호전되었다[12]. Walter 등[23]은 다기관 전향 연구에서 수술 고위험군의 급성 담낭염 환자 30명을 대상으로 EUS-GBD를 시행하였고, 기술적 성공률 90% (27/30), 임상적 성공률 96.3% (26/27)를 보고하였다. 평균 364일 간의 스텐트 유치 기간 동안 LAMS 관련 합병증은 발생하지 않았다. 최근 체계적 문헌 고찰에 따르면, 급성 담낭염에서 LAMS를 이용한 EUS-GBD의 기술적 성공률은 95.2%, 임상적 성공률은 96.7%였다[24].
4) 내시경 초음파 유도하 간위연결술(EUS-guided hepaticogastrostomy, EUS-HGS)
EUS-HGS에서 LAMS는 스텐트 직경이 짧고 플랜지가 크기 때문에 추천되지 않으며, 완전 피막형 금속 스텐트 역시 간내 담도의 분지 폐쇄를 유발할 수 있고, 금속 스텐트의 단축(shortening)에 의한 근위부 스텐트 이탈은 담즙 누출과 복막염의 위험이 있다는 문제가 있다. 이러한 제한점을 극복한 대표적인 스텐트로 양방향 고정용 플랜지를 적용한 부분 피막형 스텐트인 hybrid metal stent가 있다[7]. 10명의 환자를 대상으로 한 예비 연구에서 hybrid metal stent를 이용한 EUS-HGS의 기술적 성공률과 임상적 성공률은 모두 100%였으며, 이상반응은 기복증 2건과 출혈 1건이 있었다[7]. 21명의 환자를 대상으로 한 장기간 추적 관찰 전향 연구에서 기술적 성공률 100%, 임상적 성공률 85.7%, 조기 이상반응 19%였고, 평균 스텐트 개존 기간은 166.3일(95% 신뢰구간 94.7-237.9)이었다[25]. 또 다른 부분 피막형 스텐트인 GIOBOR를 이용한 연구에서는 110명의 환자에서 기술적 성공률 100%, 기능적 성공률 94%, 이상반응률 25%를 보고하였으며, 이상반응 중 절반은 경미한 발열과 복통이었다[8]. 재발성 담도 폐쇄는 전체 환자의 33%에서 중앙 기간 6.3개월 후에 발생하였고, 재시술은 92%에서 성공적이었다. Umeda 등[11]은 EUS-HGS를 위해 개발된 플라스틱 스텐트인 Through & Pass IT type stent를 이용한 EUS-HGS에서 5개월 추적 관찰 기간 동안 스텐트 폐쇄율 13.7%, 중앙 스텐트 개존 기간 4개월을 보고하였다. 누공 형성 후에는 누공을 통한 재시술이 가능함이 보고되었다[26].
5) 내시경 초음파 유도하 총담관십이지장연결술(EUS-guided choledochoduodenostomy, EUS-CDS)
EUS-CDS에서는 담즙 누출의 위험으로 인해 부분 피막형 스텐트는 추천되지 않고, LAMS가 선호된다. Kunda 등[27]은 57명의 절제 불가능한 악성 원위부 담도 협착 환자를 대상으로 한 후향 연구에서 AXIOS 또는 HOT-AXIOS를 이용한 EUS-CDS의 기술적 성공률 98.2%, 임상적 성공률 96.4%, 주요 합병증 발생률 7%를 보고하였다. Tsuchiya 등[28]은 다기관 전향연구로 19명의 절제 불가능한 악성 담도 폐쇄 환자에서 AXIOS를 이용한 EUS-CDS를 시행하여 임상적 성공률 95%를 보고하였다. 중앙값 184일 동안 스텐트 폐쇄는 5명에서 발생하였으며, 이상반응은 36.8%에서 경미한 수준에서 발생하였다. Jacques 등[29]은 52명의 환자를 대상으로 한 후향 연구에서 HOT-AXIOS를 이용한 EUS-CDS의 기술적 성공률 88.5%, 임상적 성공률 100%, 장기간 이상반응률 13.5% (종양에 의한 스텐트 폐쇄 4건, sump syndrome 1건, 스텐트 이탈 1건)를 보고하였다. Anderloni 등[30]은 46명의 환자를 대상으로 한 후향 연구에서 HOT-AXIOS를 이용한 EUS-CDS의 기술적 성공률 93.5%, 임상적 성공률 97.7%, 이상반응 11.6% (치명적 출혈 1건, 스텐트 폐쇄 3건, 스텐트 이탈 1건)를 보고하였다. Teoh 등[31]은 전향적 코호트 연구로서 SPAXUS를 이용한 26명의 EUS-CDS에서 기술적 성공률 88.5%와 임상적 성공률 88.9%, 장기간 이상반응 3.8%를 보고하였다.
결 론
내시경 초음파 유도하 중재시술은 기존의 침습적인 치료를 대체할 수 있는 치료로서 주목받고 있다. 최근 내시경 초음파 유도하 중재시술에 특화된 다양한 스텐트가 개발되었고 초기 연구 결과들이 고무적인 성적을 보여주고 있어 앞으로도 발전 가능성이 기대된다. 시술의 성적을 향상시키기 위해서는 시술에 특화된 스텐트의 개발뿐 아니라 유도철사, 확장용 기구 등 부속 기구의 개발이 수반되고, 시술의 표준화와 적절한 교육(training) 등이 뒷받침되어야 할 것이다. 무엇보다 시술의 적절한 적응증 확립과 근거 수립을 위한 전향적 장기 추적 관찰 연구가 필요할 것으로 생각된다.